
| A. | 一般的滴管(不是在滴瓶上的滴管)用完后要立即用水洗净,平放在实验台上 | |
| B. | 滴瓶上的滴管用完后不要用水冲洗,可直接插在原瓶中 | |
| C. | 向试管内滴加液体时,胶头滴管应伸入试管内 | |
| D. | 取液后的液管不能倒置,但可平放 |
分析 根据使用胶头滴管滴加少量液体的方法、注意事项、滴瓶上的滴管的使用方法,进行分析判断.
解答 解:A、一般的滴管(不是在滴瓶上的滴管)用完后要立即用水洗净,但不能平放在实验台上,故选项说法错误.
B、滴瓶上的滴管使用后直接插回原瓶,不能用水清洗,否则试剂瓶中的溶液将被稀释,故选项说法正确.
C、使用胶头滴管滴加少量液体的操作,注意胶头滴管不能伸入到试管内或接触试管内壁,应垂直悬空在试管口上方滴加液体,防止污染胶头滴管,故选项说法错误.
D、取液后的液管不能倒置,也不能平放,以防止污染胶头,故选项说法错误.
故选:B.
点评 本题难度不大,了解胶头滴管的使用方法、滴瓶上的滴管的使用方法、注意事项等等是正确解答本题的关键.


 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案 全程金卷系列答案
全程金卷系列答案科目:初中化学 来源: 题型:解答题
| 溶液中溶质的质量分数/% | 4 | 12 | 16 | 24 | 28 |
| 硫酸溶液的密度/g/ml | 1.02 | 1.08 | 1.11 | 1.17 | 1.20 |
| 氨水的密度/g/ml | 0.98 | 0.95 | 0.94 | 0.91 | 0.90 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 如图是甲、乙、丙三种固体物质的溶解度曲线.在20℃时,分别将等质量的三种物质的饱和溶液放入三只烧杯中,然后向溶液中分别加入等质量的相应固体物质,再将温度升高到40℃,结果甲物质全部溶解,丙物质部分溶解,试回答下列问题
如图是甲、乙、丙三种固体物质的溶解度曲线.在20℃时,分别将等质量的三种物质的饱和溶液放入三只烧杯中,然后向溶液中分别加入等质量的相应固体物质,再将温度升高到40℃,结果甲物质全部溶解,丙物质部分溶解,试回答下列问题查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
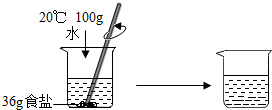 NaCl、Na2CO3、NaHCO3、CaCO3是生活中常见的盐,为学习鉴别他们的方法,老师拿来了标有A、B、C、D的这四种白色固体,并提供以下资料.
NaCl、Na2CO3、NaHCO3、CaCO3是生活中常见的盐,为学习鉴别他们的方法,老师拿来了标有A、B、C、D的这四种白色固体,并提供以下资料.| 温度 溶解度 盐 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ |
| Na2CO3 | 7.0g | 12.5g | 21.5g | 39.7g | 49.0g |
| NaHCO3 | 6.9g | 8.1g | 9.6g | 11.1g | 12.7g |
| 设计者 实验步骤 | 1 | 2 | 3 |
| 小芳 | 加盐酸 | 溶解 | 加热 |
| 小明 | 溶解 | 加盐酸 | 加盐酸 |
| 小刚 | 溶解 | 加石灰水 | 加热 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com