
【题目】如图是测定空气中氧气含量的装置,请回答下列问题:
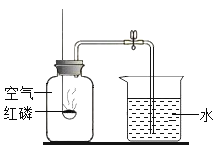
(1)点燃燃烧匙中的红磷,插入集气瓶中,红磷继续燃烧,写出红磷在集气瓶中发生反应的文字表达式为____________。
(2)冷却后,打开止水夹,可观察到的现象是__________,说明氧气约占空气总体积的________。
(3)瓶内剩余的气体主要是氮气,由该实验可得出氮气______(填“易”或“难”)溶于水和化学性质_________(填“活泼”或“不活泼”)的结论。
(4)实验过程中,燃烧匙内盛放过量的红磷的目的是______________。
(5)若红磷换成炭粉,该实验但能否获得成功?___________,理由是______________。
【答案】红磷+氧气![]() 五氧化二磷 水进入集气瓶内约占集气瓶体积的1/5 1/5 难 不活泼 使瓶内氧气全部反应完 不能 生成物是气体,瓶内压强不变小
五氧化二磷 水进入集气瓶内约占集气瓶体积的1/5 1/5 难 不活泼 使瓶内氧气全部反应完 不能 生成物是气体,瓶内压强不变小
【解析】
(1)红磷和氧气反应生成五氧化二磷,文字表达式为:红磷+氧气![]() 五氧化二磷 ;
五氧化二磷 ;
(2)冷却后,打开止水夹,可观察到的现象是:烧杯里的水被吸入集气瓶中,进入集气瓶水的体积约占集气瓶中空气总体积的五分之一;说明氧气约占空气总体积的五分之一;
(3)瓶内剩余的气体主要是氮气,由该实验可得出氮气难溶于水和化学性质不活泼的结论;
(4)实验过程中,燃烧匙内盛放过量的红磷的目的是:使瓶内氧气全部反应完;
(5)若红磷换成炭粉,该实验不能获得成功,因为木炭燃烧生成二氧化碳,二氧化碳是气态,瓶内压强不变小,使水不能被吸入集气瓶。


科目:初中化学 来源: 题型:
【题目】过氧化钠(化学式为Na2O2)可用在呼吸面具中作为氧气来源.Na2O2能跟CO2反应生成O2和另一种固体化合物(用X表示);它也能跟H2O反应生成O2 , 化学方程式为:2Na2O2+2H2O═4NaOH+O2↑.以下是某兴趣小组进行的探究活动,请回答有关问题
 .
.
(1)利用如下图所示实验装置制取氧气,看到C中溶液变浑浊,表明________.
(2)若带火星的木条复燃,能否说明CO2能与Na2O2反应生成O2, 为什么?________.若木条不复燃能否说明反应没有氧气生成,为什么?________
(3)有同学猜想X可能是酸、碱或盐中的一种.通过对物质组成的分析,大家一致认为X肯定不是酸和碱,理由是________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为了探究氢氧化钡溶液和硫酸钠溶液反应后所得滤液X的成分,同学们做了以下实验:取50克滤液于烧杯中,先向烧杯中滴加溶质质量分数为6%的硫酸镁溶液20克,接着向烧杯中滴加稀硫酸。加入溶液的质量与烧杯内沉淀的质量关系如图所示。
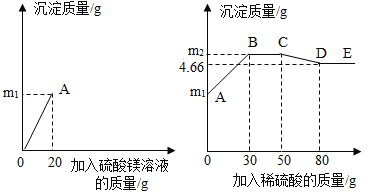
(1)滤液X的pH______7(选填“大于”、“等于”或“小于”)
(2)CD段发生反应的化学方程式为______。
(3)滤液X中含有的溶质是______。
(4)滴加入30克稀硫酸时,烧杯中沉淀的质量m2的值为多少______?(写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某物质R完全燃烧的化学方程式为:R+3O2 ![]() 2 CO2 + 3 H2O
2 CO2 + 3 H2O
有关该反应,有下列说法:
①R一定由碳、氢、氧三种元素组成
②R一定由碳、氢二种元素组成,可能含有氧元素
③R中氢元素的质量分数是最小
④R的相对分子质量等于46
⑤若4.6 g R完全燃烧生成8.8 g CO2,同时还生成了5.4 g H2O
其中正确说法的个数有( )
A.2个 B.3个 C.4个 D.5个
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在“质量守恒定律”的课堂教学中,老师引导同学们进行“化学反应中,反应物与生成物的质量关系”的实验探究.他们使用的实验装置和选用药品如图所示,现分别以A、B、C、D表示如下:
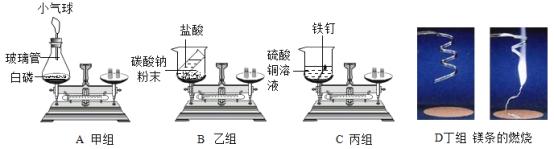
A、B、C、D四个实验分别由甲、乙、丙、丁四个组的同学来完成,他们都进行了规范的操作、准确的称量和细致的观察。
(1)A实验:锥形瓶底放层细沙的原因是:______;小气球的作用是:______;白磷刚引燃,立即将锥形瓶放到天平上称量,天平不平衡。结论是:质量不守恒。待锥形瓶冷却后,重新放到托盘天平上称量,天平平衡。结论是:质量守恒.你认为结论正确的是______(填“前一种”或“后一种”),而导致另一种结论错误的原因是:______。
(2)丙组同学认为C实验说明了质量守恒定律。请你从原子的角度说明为什么?______.
(3)如果A装置中只是将药品改为少量的二氧化锰和过氧化氢,反应前后天平仍不平衡,原因是:______;结论是:参加反应的过氧化氢的质量一定______(填“等于”或“不等于”)生成的水和氧气的质量总和。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】燃料的发现和利用提高了人类生活的质量,推动了人类文明的进步。
(1)将煤隔绝空气加强热,得到焦炭、煤气等,该过程属于______(填“物理”或“化学”)变化。
煤与高温水蒸气反应生成CO和![]() 在300℃、1.5MPa、催化剂存在的条件下,CO和
在300℃、1.5MPa、催化剂存在的条件下,CO和![]() 可转变为液体燃料甲醇
可转变为液体燃料甲醇![]() 。写出CO与
。写出CO与![]() 反应生成甲醇的化学方程式:_______。
反应生成甲醇的化学方程式:_______。
(2)焦炭(主要成分是碳)是高炉炼铁的重要原料。炼铁高炉内发生的主要化学反应如图1所示,其中反应②体现了焦炭的_______性。
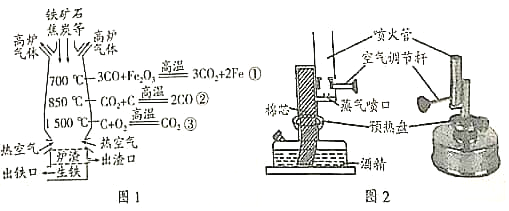
(3)乙醇可作为酒精灯、酒精喷灯或灯的燃料。某钢质酒精喷灯的结构如图2所示。使用酒精喷灯时,先在预热盘中注入酒精并点然,一段时间后,调节空气调节杆,即可点燃酒精喷灯。结合燃烧的条件回答:点燃预热盘中酒精的目的是_______。
(4)氢气的制取和储存越来越受到人们的关注。
①最理想的制氢方法:在合适的催化剂作用下,利用太阳光使水分解。该制氢过程______(填“吸收”或“放出”)能量,生成的氢气与氧气在相同条件下的体积之比为______。
②我国稀土资源丰富,某种稀土储氢材料(用M表示)的储氢原理可表示为![]() 。M的化学式为______。
。M的化学式为______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我国制碱工业采用联合制碱法生产纯碱,其反应原理如下:NaCl+NH3+H2O+CO2=NaHCO3↓+NH4C1;2NaHCO3![]() Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑
(资料阅读)
①通常情况下,浓氨水具有较强的挥发性,易挥发出氨气。氨气是一种无色有刺激性气味的气体,极易溶于水,排放到空气中会污染空气。
②饱和碳酸氢钠溶液不能吸收二氧化碳。
化学兴趣小组在实验室模拟联合制碱法进行了如下实验:
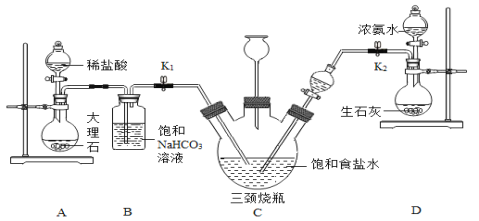
Ⅰ.关闭K1,先打开K2通入NH3,调节气流速率,待其稳定后,再打开K1通入CO2。
Ⅱ.待三颈烧瓶内出现较多固体时,关闭K2停止通入NH3;一段时间后,关闭K1停止通入CO2。
Ⅲ.将三颈烧瓶内反应后的混合物过滤,将滤出的固体洗涤、低温干燥,得到碳酸氢钠固体。再将其加热使其完全分解即得纯碱。
请回答下列问题。
(1)写出A装置中反应的化学方程式______。
(2)B装置中饱和碳酸氢钠溶液的作用是______。
(3)D装置中生石灰的作用是______。
(4)C装置中长颈漏斗的作用除了随时添加饱和食盐水,还有______作用。有同学认为应该在长颈漏斗内放置浸有稀硫酸的棉花团,其目的是______。
(5)关闭K2停止通入NH3,还要继续通入一段时间CO2,其目的是______。
(6)写出副产品氯化铵和熟石灰反应的化学方程式______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组的同学对蜡烛的燃烧和空气中氧气含量的测定进行了一系列的探究,请你参与并回答下列问题。
(发现问题1)点燃蜡烛,发现蜡烛火焰的明亮程度不一样,是什么原因所致呢?
[猜想与假设1)猜想①:蜡烛中可燃物成分不一样;
猜想②:_____。
(发现问题2)同学们用蜡烛代替红磷测定空气中氧气的含量,发现蜡烛熄灭后,回流到集气瓶中的水远小于瓶容积的五分之一.是什么原因所致呢?
(猜想与假设2)猜想①:蜡烛燃烧产生CO2气体;
猜想②:_____。
猜想③:_____。
(实验验证)将蜡烛点燃后用氧气传感器定量测定瓶中的氧气含量,数据如图1。
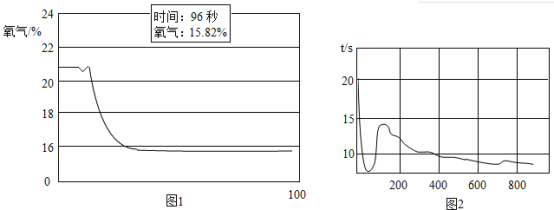
(深入探究)蜡烛燃烧产生的CO2可能是影响蜡烛熄灭的主要原因.请你设计方案证明集气瓶中蜡烛燃烧生成的是CO2:_____
(拓展探究]某同学用氧气传感器定量测定密闭条件下足量红磷燃烧时氧气的含量变化,如图2,在110秒时氧气的含量有所上升,接着再慢慢下降最终维持在8.85%左右.你对氧气最终含量不是0%而是8.85%左右是怎么理解的?_____
对比蜡烛和红磷实验的结果,发现用红磷实验时密闭容器中最终氧气的含量更低,对此你有什么认识?_____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下列“制取蒸馏水”的实验装置改进,回答有关问题:
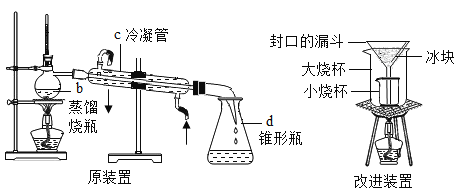
(1)两套装置中作用相当的仪器:漏斗与_____(填“b”“c”或“d”)。
(2)装置改进后,下列说法正确的是_____(填序号,双选)。
A 同样可以降低水的硬度
B 冰块与水的性质完全相同
C 比原装置得到的蒸馏水更纯
D 利用太阳光、塑料袋、矿泉水瓶等作代替品可户外自制饮用水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com