
【题目】某化学实验小组在验证酸碱盐的化学性质时,做如图所示的实验
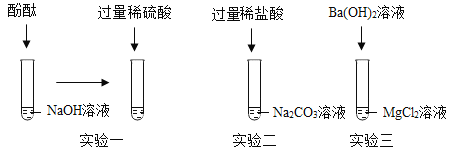
(1)实验一能够观察到的明显现象是_____。
(2)实验二发生反应的化学方程式为___。
(3)将上述试验后三只试管中所有的物质倒入一个烧杯中,充分混合后过滤。得到白色固体A和无色溶液B,向滤液B中滴加少量Ba(OH)2溶液,无现象,综上所述,固体A的成分是____,溶液B中除酚酞外,一定还含有的溶质是____。
【答案】溶液由无色变成红色,再由红色变为无色 Na2CO3+2HCl=2NaCl+H2O+CO2↑ BaSO4 NaCl、HCl、MgCl2
【解析】
(1)实验一:酚酞遇碱性溶液变红,与酸性溶液为无色,氢氧化钠与稀硫酸反应产生硫酸钠,硫酸过量,混合溶液显酸性,则能够观察到的明显现象是溶液由无色变成红色,再由红色变为无色。
(2碳酸钠与稀盐酸反应产生氯化钠、水和二氧化碳的化学方程式为:Na2CO3+2HCl=2NaCl+H2O+CO2↑;
(3)实验一:氢氧化钠与过量的稀硫酸反应产生硫酸钠溶液,剩余稀硫酸;
实验二:过量的稀盐酸与碳酸钠反应产生氯化钠溶液,剩余稀盐酸;
实验三:氢氧化钡与氯化镁反应产氢氧化镁沉淀和氯化钡溶液,还可能还有氢氧化钡或氯化镁;
将上述试验后三只试管中所有的物质倒入一个烧杯中,充分混合后过滤。得到白色固体A和无色溶液B,白色固体A可能为:硫酸钡沉淀或氢氧化镁沉淀;溶液B中含有酚酞为无色,则说明溶液显酸性(或中性);向滤液B中滴加少量Ba(OH)2溶液,无现象,说明溶液B中没有稀硫酸和硫酸钠,因为氢氧化钡与稀硫酸(或硫酸钠)都能产生硫酸钡沉淀,溶液B中没有氯化镁,因为氯化镁与氢氧化钡反应产生氢氧化镁沉淀,加入少量的氢氧化钡(显碱性)溶液不变色,说明溶液显酸性,一定有盐酸;则白色固体A是硫酸钡(不溶于酸);不是氢氧化镁,因为氢氧化镁的能与酸反应,综上所述,固体A的成分是:硫酸钡,溶液B中除酚酞外,一定还含有的溶质是:氯化钠、氯化镁、氯化氢。


科目:初中化学 来源: 题型:
【题目】类比推理在化学学习和科学研究中有重要意义,下列说法正确的是
A.碱的溶液显碱性,所以显碱性的溶液都是碱溶液
B.化合物中含不同种元素,所以含不同种元素的物质都是化合物
C.H2、C、CO都具有还原性,所以它们都能与氧化铜发生置换反应
D.浓硫酸、氢氧化钠、氧化钙都是干燥剂,所以它们都能用于干燥氧气
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】分析下列化学反应,回答有关问题:
① ![]()
② ![]()
(1)分析总结以上两个反应的规律是:碱与含铵根离子的盐反应都生成盐、水和_________________。
(2)标出硝酸铵中氮元素的化合价________________。
(3)根据以上两个方程式的反应规律写出氢氧化钙与氯化铵反应的化学方程式:_____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】活性炭可用于净水,其净水原理是_____。新型自来水消毒剂CIO2可由如下的反应制取: ![]() ;则X的化学式为_____;工业上高炉炼铁的原理(以磁铁矿为例,用化学方程式表示)_____。
;则X的化学式为_____;工业上高炉炼铁的原理(以磁铁矿为例,用化学方程式表示)_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】程伟同学将浑浊的湖水样品倒入烧杯中,先加入明矾粉末搅拌溶解,静置一会儿后,采用下图所示装置进行过滤,请问:
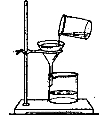
(1)图中还缺少的一种仪器是_________________ 。
(2)过滤后观察发现,滤液仍然浑浊。可能的原因之一______________________:
(3)改进后过滤,得到了澄清透明的水,若要制取纯水,还需采用的净化方法是___________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水是生命之源,保护水环境,珍爱水资源,回答下列与水有关的问题
(1)写出生活中一种节约用水的具体做法_________________________。
(2)下列实验中,对水的主要作用分析不全面的是_____________。(填字母)
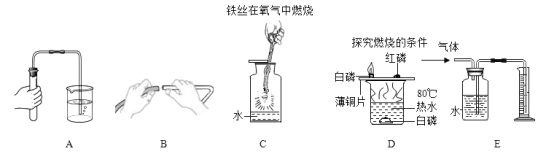
A液封形成密闭体系
B润湿玻璃管口便于插入
C防止熔融物溅落炸裂集气瓶
D提供热量
E测量气体的体积
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】向一定质量的Na2SO4、MgSO4混合溶液中先后滴加150.0g 3.42%的稀Ba(OH)2溶液、100.0g稀H2SO4,产生沉淀的质量与滴加的溶液质量关系如下图所示。下列说法不正确的是( )
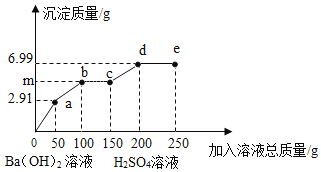
A. a点沉淀的成分为一种
B. 向e点所得溶液中滴加紫色石蕊试液,溶液呈红色
C. m=5.24
D. 所用稀H2SO4的质量分数为3.92%
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】以粗盐为原料生产ClO2(可用于自来水消毒)的工艺主要包括:①粗盐精制;②电解微酸性NaCl溶液;③ClO2的制取。工艺流程如下图,其中反应Ⅲ制取ClO2的化学方程式为2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O。
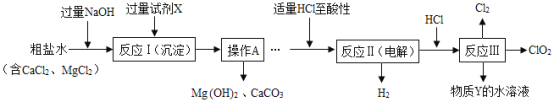
(1)试剂X是_____(填化学式);操作A的名称是_____。
(2)加入适量HCl除为了满足电解时的微酸性外,还能除去溶液中的杂质离子,其中所发生的中和反应的化学方程式:_____。
(3)为提高经济效益,生产过程中除将H2和Cl2制成HCl充分利用外,还可循环使用的物质Y是_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com