
【题目】如图是A、B两种固体物质的溶解度曲线。
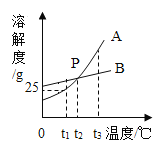
(1) P点含义______________。
(2)A中含有少量B,提纯A的方法______________。
(3) t1°C时,25gA溶解在100g水中所形成溶液的溶质质量分数(填“>”、“=”或“<”)____________25%
(4) t3°C时,将等质量的A、B两种物质的饱和溶液分别降温至t1°C,所得溶液中溶剂质量的大小关系是______________。
【答案】t2°C时,A和B的溶解度相等 降温结晶 < B>A(或A<B)
【解析】
(1)P点是A、B两曲线在t2°C的一个交点,含义是t2°C时,A和B的溶解度相等。
(2)A、B两物质的溶解度都随温度的升高而增大,且A的溶解度受温度影响变化比较大,A中含有少量B,提纯A的方法降温结晶。
(3)t1°C时,A的溶解度为25g,25g A可以完全溶解在100g水中,所形成溶液的溶质质量分数为![]() ,20% < 25%。
,20% < 25%。
(4)t3°C时,A的溶解度大于B的溶解度,所以在等质量的A、B两种物质的饱和溶液中,A的溶质质量大于B的溶质质量,则B的溶剂质量大于A的溶剂质量,当温度降至t1°C,两溶液析出晶体,溶质质量减少,但溶剂质量不变,因此所得溶液中溶剂质量的大小关系是B>A。


 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案科目:初中化学 来源: 题型:
【题目】实验是学习和研究化学的重要方法。回答问题。
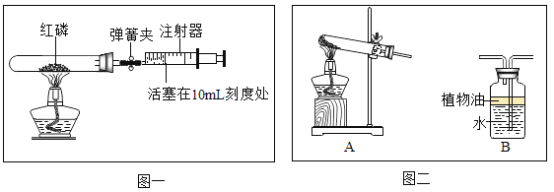
(1)图一装置可测定空气中氧气的含量,实验的主要操作步骤如下∶①将过量红磷平装入试管中,将20mL的注射器活塞置于10mL刻度处,并按图一所示的连接方式固定好,再将弹簧夹紧橡皮管;②点燃酒精灯;③撤去酒精灯,待试管冷却后松开弹簧夹;④读取注射器活塞的数据。注射器活塞将从10mL刻度处慢慢前移到约为_____________mL刻度处才停止。(已知试管容积为35 mL,不考虑红磷和五氧化二磷的体积对试管中空气体积的影响)
(2)用图二中的装置A制取氧气的化学反应方程式为_____________。组装发生装置A时,下列仪器、用品的组装顺序是____________(填序号)。
a 试管
b 酒精灯
c 铁架台
d 木块
(3)图二中的装置B ____________(填“能”或“不能”)用来收集CO2。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是微型实验的装置图。
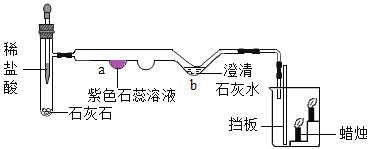
(1)由烧杯中变化的现象可得出二氧化碳具有什么性质?____________________
(2)写出b处发生反应的化学方程式_____________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是甲、乙、丙三种物质的溶解度曲线,下列说法错误的是( )

A.甲中混有少量杂质乙,可采用降温结晶的方法进行提纯
B.t3℃时,将甲、丙的饱和溶液降温,甲溶液溶质的质量分数减小,丙不变
C.t2℃时,甲、丙溶液中溶质的质量分数甲>丙
D.t1℃时,60g水中溶解18g甲可得到其饱和溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据如图所示实验回答问题:
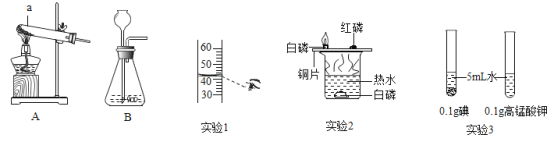
(1)装置A中仪器a的名称是_____。
(2)实验室用装置B制取氧气的反应方程式是_____。
(3)在配制一定溶质质量分数的氯化钠溶液时, 量取水的操作如实验1所示,所配溶液的溶质质量分数会_____,(填“偏大”或“偏小”)。
(4)实验2中热水的作用是_____。
(5)实验3所得的结论是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为测定混有少量氯化钠的纯碱中碳酸钠的质量分数,做如下实验:准确称量样品12g,向其中加入68g稀盐酸,恰好完全反应,称量所得溶液质量为75.6g。请计算: (计算结果精确到小数点后一位)
(1)反应生成二氧化碳的质量___________。
(2)纯碱样品中碳酸钠的质量分数____________。
(3)所得溶液中溶质的质量____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学是以实验为基础的科学,实验是科学探究的重要手段。
(1)根据下图所给装置回答问题:
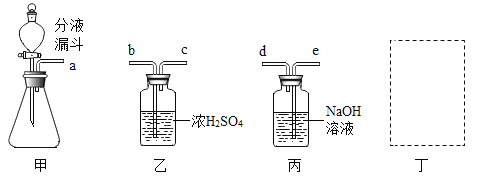
①若实验室用甲装置制取氧气,其原理化学方程式是________________。
②用集气瓶采用排空气法收集氧气,请在丁处方框中画出装置图________________ (只画集气瓶和导气管)。
③锌跟稀盐酸反应制得的氢气中常带有少量的HCl气体和水蒸气,若欲用乙、丙装置净化除杂得到纯净、干燥的氢气,那么乙、丙装置的导管连接顺序是____________。
(2)下图是二氧化碳的制取微型装置图,请回答。
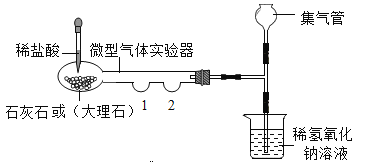
①在装置“1”处放置试剂____________,用来验证制取的气体是二氧化碳;若在“2”处盛放有少量的紫色石蕊试剂,那么发生的现象是__________________。
②用橡胶塞塞紧集气管口,挤压胶头滴管,二氧化碳气体进入氢氧化钠溶液,反应的化学方程式是______________;请设计实验证明氢氧化钠没有完全反应______________。
(3)将12.5g石灰石放入盛有150g稀盐酸的烧杯中恰好反应(假设石灰石样品中杂质不与稀盐酸反应也不溶于水),称量烧杯中物质总质量是158. 1g.求该石灰石中碳酸钙的质量分数是__________?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】味精是生活中的调味品。味精的鲜味来自于主要成分“谷氨酸钠”(化学 式是C5H8NO4Na,易溶于水,与AgNO3不反应),另外还含有NaCl及其它成分。
(1)实验表明,味精在100 °C时加热半小时,只有0. 3%的味精(谷氨酸钠)生成焦谷氨酸钠(有毒),对人体的影响甚微。对此,下列认识正确的是________________________。
a 味精不能吃,对人体有害
b 尽量避免在菜肴温度较高时使用味精
c 生成焦谷氨酸钠的过程是物理变化
d 实验是研究问题的一种有效方法
(2)称取5.0 g味精配制成50 g溶液,量取蒸馏水的量筒规格是__________________。
a 10 mL b 50 mL c 100 mL
(3)如图是配制过程,正确的操作顺序为_________ (填序号)。
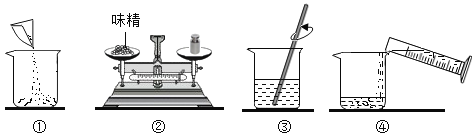
(4)为测定味精中NaCl的质量分数,进行如下实验:向上述配制好的溶液中加入AgNO3溶液至_______。反应的化学方程式是____。过滤后得沉淀质量为2.87 g,则该味精中NaCl的质量分数为______。
(5)实验后对比味精袋上的标签,发现所测得的NaCl的质量分数偏高,则可能的原因是____(填字母)。
a 配制溶液时仰视量水
b 反应中加入的AgNO3溶液过量
c 洗涤、干燥沉淀不彻底
d 味精中有其它能与AgNO3反应生成沉淀的物质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com