
·ÖĪö øł¾ŻĢ¼ĖįÄĘÄÜÓėĀČ»Æ±µ·“Ӧɜ³ÉĮĖĢ¼Ėį±µ³Įµķ£¬Ķعż²ā¶ØĢ¼Ėį±µµÄÖŹĮææÉĒó³öĢ¼ĖįÄʵÄÖŹĮ棬æɲā³ö¼īĆęÖŠNa2CO3µÄŗ¬ĮæŹĒ·ńŅŖĒó£»ŅŖ¼ĘĖćNa2CO3ŗ¬Į棬¾ĶŠčŅŖ³ĘĮæĢ¼Ėį±µ³ĮµķµÄÖŹĮ棬øł¾ŻĢ¼Ėį±µµÄÖŹĮæĒóĢ¼ĖįÄʵÄÖŹĮ棻Čē¹ūĢ¼ĖįÄʵÄŗ¬ĮæµČÓŚ96%£¬ÄĒĆ“Ģ¼ĖįÄʵÄÖŹĮæ=1g”Į96%=0.96g£¬øł¾ŻNa2CO3+CaCl2=CaCO3”ż+2NaCl¼ĘĖć¼“æÉ£®
½ā“š ½ā£ŗ£Ø1£©ÓÉÉĻ·ÖĪöæÉÖŖ£¬¼ģ²āµÄŌĄķŹĒ£ŗNa2CO3+BaCl2=BaCO3”ż+2NaCl£»
£Ø2£©ÓÉÓŚĢ¼ĖįÄĘÄÜÓėĀČ»Æ±µ·“Ӧɜ³ÉĮĖĢ¼Ėį±µ³Įµķ£¬Ķعż²ā¶ØĢ¼Ėį±µµÄÖŹĮææÉĒó³öĢ¼ĖįÄʵÄÖŹĮ棬æɲā³ö¼īĆęÖŠNa2CO3µÄŗ¬ĮæŹĒ·ńŅŖĒó£»¾ĶŠčŅŖ³ĘĮæĢ¼Ėį±µ³ĮµķµÄÖŹĮ森ĖłŅŌ£¬Ń”ŌńĖłŠčŅ©Ę·ŹĒĖ®ŗĶĀČ»Æ±µČÜŅŗ£¬Ó¦²āĮæµÄŹż¾ŻŹĒĢ¼Ėį±µµÄÖŹĮ棻
£Ø3£©Čē¹ūĢ¼ĖįÄʵÄŗ¬ĮæµČÓŚ96%£¬ÄĒĆ“Ģ¼ĖįÄʵÄÖŹĮæ=1g”Į96%=0.96g£¬ÉčĢ¼ĖįøʵÄÖŹĮæĪŖx£»
Na2CO3+BaCl2=BaCO3”ż+2NaCl
106 197
0.96g x
$\frac{106}{0.96g}=\frac{197}{x}$ ½āµĆ£ŗx”Ö1.78g
µ±±»²āĮæµÄ³ĮµķµÄŹż¾Ż”Ż1.78g£¬”°Na2CO3ŗ¬Įæ”Ż96%”±Ź±ŹĒÕꏵæɊŵģ®
µćĘĄ ±¾æ¼µć¼Čæ¼²éĮĖŹµŃé²½ÖčµÄÉč¼Ę£¬ÓÖæ¼²éĮĖ»Æѧ·½³ĢŹ½µÄŹéŠ“£¬»¹¶ŌŹµŃé½ųŠŠĮĖĘĄ¼Ū£¬×ŪŗĻŠŌ±Č½ĻĒ森ŹµŃéĢ½¾æĢāŹĒ½ü¼øÄźÖŠæ¼µÄČȵćÖ®Ņ»£¬Ėü°üĄØŹµŃé·½·ØŗĶ¹ż³ĢµÄĢ½¾æ£¬ŹµŃé½įĀŪŗĶŹµŃé¹ęĀɵÄĢ½¾æµČ£®±¾ĢāĶعżŹµŃé׏ĮĻŗĶŹµŃé·ÖĪö£¬µĆµ½ĮĖÕżČ·µÄ½įĀŪ£¬ŹōÓŚ½įĀŪŠŌĢ½¾æ£®Ķ¬Ń§ĆĒŅŖ¾ßĢå·ÖĪö£¬×ŪŗĻÕĘĪÕ£®


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
 Šķ¶ąĪļÖŹŌŚČÜŅŗÖŠ¶¼ŅŌĄė×ÓŠĪŹ½“ęŌŚ£®ĪŅĆĒŹģĻ¤µÄø“·Ö½ā·“Ó¦¾ĶŹĒČÜŅŗÖŠĄė×Ó¼ä½įŗĻµĆµ½Ė®”¢ĘųĢå»ņ³ĮµķµÄŅ»Ąą»Æѧ·“Ó¦£®Čē£ŗĒāŃõ»ÆÄĘÓėŃĪĖįµÄ·“Ó¦¾ĶŹĒČÜŅŗÖŠµÄH+ŗĶOH-½įŗĻ³ÉĖ®·Ö×ӵĹż³Ģ£ØČēĶ¼ĖłŹ¾£©£®½įŗĻŠÅĻ¢”¢Ķ¼Ź¾£¬ÄćČĻĪŖĻĀĮŠø÷×éĄė×Ӽ䲻ÄÜ·“Ó¦µÄŹĒ£Ø””””£©
Šķ¶ąĪļÖŹŌŚČÜŅŗÖŠ¶¼ŅŌĄė×ÓŠĪŹ½“ęŌŚ£®ĪŅĆĒŹģĻ¤µÄø“·Ö½ā·“Ó¦¾ĶŹĒČÜŅŗÖŠĄė×Ó¼ä½įŗĻµĆµ½Ė®”¢ĘųĢå»ņ³ĮµķµÄŅ»Ąą»Æѧ·“Ó¦£®Čē£ŗĒāŃõ»ÆÄĘÓėŃĪĖįµÄ·“Ó¦¾ĶŹĒČÜŅŗÖŠµÄH+ŗĶOH-½įŗĻ³ÉĖ®·Ö×ӵĹż³Ģ£ØČēĶ¼ĖłŹ¾£©£®½įŗĻŠÅĻ¢”¢Ķ¼Ź¾£¬ÄćČĻĪŖĻĀĮŠø÷×éĄė×Ӽ䲻ÄÜ·“Ó¦µÄŹĒ£Ø””””£©| A£® | H+”¢Na+”¢0H-”¢NO3- | B£® | H+”¢K+”¢CO32-”¢HCO3- | ||
| C£® | Na+”¢K+”¢Cl-”¢OH- | D£® | K+”¢Ba2+”¢Cl-”¢SO42- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
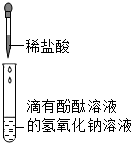 ijĶ¬Ń§½ųŠŠČēĶ¼ĖłŹ¾ŹµŃ飬֤Ć÷Ėį¼ī·¢Éś·“Ó¦µÄĻÖĻóĪŖ£ŗŹŌ¹ÜÖŠČÜŅŗÓÉŗģÉ«±äĪŖĪŽÉ«£¬øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖNaOH+HCl=NaCl+H2O£®ŹµŃéŗó²āµĆŹŌ¹ÜÖŠČÜŅŗµÄpH=2£¬øĆČÜŅŗÖŠµÄČÜÖŹ³ż·ÓĢŖĶāÓŠNaClŗĶHCl£®
ijĶ¬Ń§½ųŠŠČēĶ¼ĖłŹ¾ŹµŃ飬֤Ć÷Ėį¼ī·¢Éś·“Ó¦µÄĻÖĻóĪŖ£ŗŹŌ¹ÜÖŠČÜŅŗÓÉŗģÉ«±äĪŖĪŽÉ«£¬øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖNaOH+HCl=NaCl+H2O£®ŹµŃéŗó²āµĆŹŌ¹ÜÖŠČÜŅŗµÄpH=2£¬øĆČÜŅŗÖŠµÄČÜÖŹ³ż·ÓĢŖĶāÓŠNaClŗĶHCl£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | æÉ“ó“ó½µµĶÓĶĮĻ¼Ūøń | |
| B£® | ÓŠÖśÓŚ¼õĒį“óĘųĪŪČ¾£¬øÄÉĘ“óĘų»·¾³ | |
| C£® | ŅŅ“¼ŹĒŅ»ÖÖŌŁÉśµÄÄÜŌ“ | |
| D£® | ÓŠÖśÓŚ“Ł½ųĮøŹ³×Ŗ»Æ£¬ĢįøßÅ©ĆńŹÕČė |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com