

���� ���ݼ׳���ķ�ˮ�ʻ�ɫ���ʼ����Ȼ�����Һ�����ҷ�Ӧ����Һ�ʼ��ԣ�˵����������ʣ�࣬�������������ƣ����Ͷ���Ӧ�������ݣ��ʱ��Ͷ��������̼���Ƶķ�Ӧ��Ҫʹ�����ŷŵķ�ˮ�����ԣ��ʱ��Ͷ���Ӧ����Һ�����ԣ��ݴ˽��
��� �⣺��1�����ҷ�Ӧ�����Һ�Լ��ԣ��ҳ���ķ�ˮ��Թ�������ˮ��Һ�ʻ�ɫ�����Լ����Ȼ�����Һ���Ҿ����������ƣ�������Ӧ�����Һ�����ԣ�������ķ�ˮ���������Ա���̼���ƣ��������ᣬ�������ƺ�̼���Ʋ��ܻ�������Ϊʹ�ҡ����������ˮ��Թ��������Ͷ��ķ�Ӧ�Ͳ���������ԣ�
�ʴ�Ϊ����1��NaOH��
��2���ڢڷ�Ӧ�صķ�ˮ�е��������Ȼ��ƺ����ᣬ���NaOH��HCl��
��3���ڢ۷�Ӧ�������������ƺ����ᷴӦ�����Ȼ��ƺ�ˮ�����HCl+NaOH�TNaCl+H2O��
���� �ڽ������ʱ���ȸ���������Ӧ��������Ʋ��ˮ����ɣ�Ȼ���ٽ�����е�����������֤���ɣ�


 ��ʦ�㾦�ִʾ��ƪϵ�д�
��ʦ�㾦�ִʾ��ƪϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | 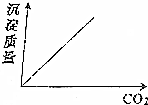 | B�� | 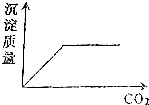 | ||
| C�� | 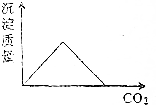 | D�� | 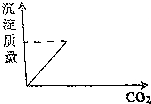 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢� | B�� | �ڢ� | C�� | �ۢ� | D�� | �٢ڢۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ������ij����һ�������С�ӣ�ˮ����ڸ�Ӫ������Ⱦ�������ͼˮ�ʼ��վ��2013��8�¶Դ�ˮ���һ��DO���ܽ�������ʵ�����ݣ��ش𣺣���֪C-12����H-1����O-16����
������ij����һ�������С�ӣ�ˮ����ڸ�Ӫ������Ⱦ�������ͼˮ�ʼ��վ��2013��8�¶Դ�ˮ���һ��DO���ܽ�������ʵ�����ݣ��ش𣺣���֪C-12����H-1����O-16����| ˮ��/�� | 25 | 26 | 27 | 29 | 31 | 32 | 34 |
| DO����ֵ/mg•L-1 | 8.15 | 8.00 | 7.85 | 7.65 | 7.43 | 7.30 | 7.20 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �� | B�� | ������ | C�� | ������ | D�� | �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 �ձ������˵�վ�����Ե��ں�Хʱ����й©��������Ԫ�ر���������֪����ͼ��Ԫ�����ڱ����ṩ�ĵ�Ԫ�صIJ�����Ϣ����ԭ�ӵĽṹʾ��ͼ��
�ձ������˵�վ�����Ե��ں�Хʱ����й©��������Ԫ�ر���������֪����ͼ��Ԫ�����ڱ����ṩ�ĵ�Ԫ�صIJ�����Ϣ����ԭ�ӵĽṹʾ��ͼ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ʵ����� | ʵ������ | ʵ����� |
| ��ȡ������Ʒb���ձ��У�����������ˮ�����ò��������� | ��Ʒȫ�ܣ��γ���ɫ��Һ | �������� |
| ���ڢٵ���Һ�м�BaCl2��Һ | ���������� | |
| ���ڢڵõ�����Һ�м�����AgNO3��Һ | �а�ɫ�������ɣ������ӵ���MgCl2 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com