
(6分)为了测定某含杂质7%的黄铜样品中铜的质量分数(杂质中不含铜、锌元素,杂质不溶于水,不与其它物质反应,受热也不分解),某化学小组进行了如下实验:

(1)配制上述质量分数为14.6%的稀盐酸,需要质量分数为36.5%的浓盐酸的质量是______;
(2)发生反应的化学方程式为____________________________________________;
(3)根据已知条件列出求解100g该黄铜样品中锌的质量(x)的比例式为__________;
(4)该黄铜样品中铜的质量分数是__________;
(5)向过滤后所得滤液中加入87.4g水,则最终所得溶液中溶质的质量分数是__________;
(6)欲将黄铜样品中的铜转化为铜盐,可将过滤后所得的不溶性物质洗涤、烘干,然后在空气中加热,充分反应,则可得到含杂质的氧化铜的质量是__________,再经过某些反应及操作就得到了所需铜盐。
 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源:2015年初中毕业升学考试(福建泉州卷)化学(解析版) 题型:探究题
(18分)为提高实验探究能力,某化学兴趣小组的同学在老师的指导下,对一瓶久置出现变质硬化的氢氧化钙固体进行如下探究活动。
【探究活动一】试验硬化的氢氧化钙样品是否完全变质
(1)用化学方程式表示氢氧化钙变质的原因: 。
(2)检验氢氧化钙样品是否完全变质,进行如下实验:
实验步骤 | 实验现象 | 实验结论 |
取氢氧化钙样品少量,研细后加适量蒸馏水 充分混合后静置, | 该样品还含有氢氧化钙 |
【探究活动二】测定样品中含有的变质固体(以下用R表示)的质量分数
取3克部分变质的氢氧化钙样品与足量的稀盐酸反应,测量生成气体的体积(气体不溶于植物油),从而计算出样品中R的质量,便可求出样品中R的质量分数。实验装置(气密性良好)如图1所示。
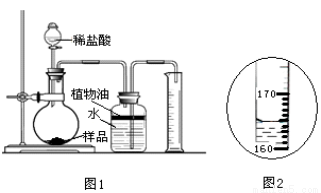
(3)将稀盐酸滴入样品中,产生气体的化学方程式为 ,反应一段时间后,当观察到 (填实验现象),才停止滴加稀盐酸。
(4)实验中量筒的作用是 。
(5)实验结束后,量筒内进入水的体积如图2所示,其读数为 mL。已知在该实验条件下,生成气体的密度为2g·L-1,通过计算,样品中R的质量分数为 。
(6)上述图1所示实验装置和相关试剂,用来实验测定样品中R的质量分数是比较粗略的,请简要说明测定数据存在误差的原因: (写一个)。
查看答案和解析>>
科目:初中化学 来源:2015年初中毕业升学考试(北京卷)化学(解析版) 题型:选择题
一种铁原子的原子核内有26个质子和30个中子,该原子的核外电子数为
A.4 B.26
C.30 D.56
查看答案和解析>>
科目:初中化学 来源:2015年初中毕业升学考试(黑龙江大庆卷)化学(解析版) 题型:填空题
(6分)(1)下列氮肥含氮量由高到低的排列顺序是: (用序号表示)
常见氮肥 | ①NH4NO3 | ②NH4HCO3 | ③CO(NH2)2 |
相对分子质量 | 80 | 79 | 60 |
(2)治理汽车尾气中的NO和CO的一种方法是:在汽车的排气管上装一个催化转化装置。使NO和CO反应生成N2和CO2,写出该反应的化学方程式 。
(3)有机物中碳氢化合物可用CxHy表示,其完全燃烧的化学方程式:
CxHy+(x+ )O2
)O2 xCO2+
xCO2+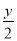 H2O
H2O
判断等质量的①CH4,②C2H2,③C2H4,三种碳氢化合物完全燃烧消耗氧气由大到小的顺序是 (用序号表示)。
查看答案和解析>>
科目:初中化学 来源:2015年初中毕业升学考试(黑龙江大庆卷)化学(解析版) 题型:选择题
下列关于反应的描述,反应方程式及反应类型完全正确的是
A.实验室用加热高锰酸钾制取氧气2KMnO4Δ K2MnO4+MnO2+O2↑ 分解反应
B.铁丝在氧气中燃烧 4Fe+3O2点燃2Fe2O3 化合反应
C.高炉炼铁原理 Fe2O3+3CO高温 2Fe+3CO2 复分解反应
D.将铁片投入足量的稀盐酸中2Fe+6HCl=2FeCl3+3H2↑ 置换反应
查看答案和解析>>
科目:初中化学 来源:2015年初中毕业升学考试(黑龙江哈尔滨卷)化学(解析版) 题型:填空题
(3分)下图是过氧化氢在一定条件下发生分解反应的微观模拟图,请回答下列问题:

(1)在C图中将相关粒子图形补充完整(用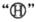 表示氢原子,用
表示氢原子,用 表示氧原子);
表示氧原子);
(2)此化学变化中没有发生改变的粒子是__________________(填名称);
(3)此反应后生成的B与C中物质质量的最简整数比为_______________。
查看答案和解析>>
科目:初中化学 来源:2015年初中毕业升学考试(黑龙江哈尔滨卷)化学(解析版) 题型:选择题
对下列事实的解释正确的是
选 项 | 事 实 | 解 释 |
A | 一氧化碳和二氧化碳的化学性质不同 | 一个二氧化碳分子比一个一氧化碳分子多一个氧原子 |
B | 稀盐酸、稀硫酸均显酸性 | 溶液中都含有氢元素 |
C | 用水银温度计测量体温 | 温度升高,分子间间隔变大 |
D | 冰水混合物属于纯净物 | 都含有相同原子 |
查看答案和解析>>
科目:初中化学 来源:2015年初中毕业升学考试(海南卷)化学(解析版) 题型:填空题
铝是生活中常见的金属。
(1)金属铝常用做导线是利用它的 性;
(2)金属铝表面常有一层致密的氧化膜,氧化膜主要成分是 (填名称或化学式);
(3)资料显示:铝与氢氧化钠和水反应生成偏铝酸钠(NaAlO2)和氢气;用56.25g 含杂质4%的铝片(杂质对产生氢气的质量无影响)与足量的氢氧化钠和水充分反应,生成氢气的质量为 g。
查看答案和解析>>
科目:初中化学 来源:2015年初中毕业升学考试(广东揭阳卷)化学(解析版) 题型:计算题
(6分)某铝制品的主要成分是Al和Cu,课外小组将200gNaOH溶液不断地加到50g铝制品中得到如下数据(已知金属铝既可以跟强酸反应也可以与强碱反应,而金属铜不能与强碱反应,铝与NaOH溶液反应的化学方程式为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑)
实验次数 | 第一次 | 第二次 | 第三次 | 第四次 |
加入氢氧化钠溶液的质量/g | 50 | 50 | 50 | 50 |
剩余固体的质量/g | 36.5 | 23 | 9.5 | 9.5 |
请回答以下问题(1)该50g铝制品中含有 g铜。
(2)求所用氢氧化钠溶液的溶质质量分数为多少?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com