
| 反应前 | 反应后 |
| E的质量为100.0g | E的质量为102.25g |
| F的质量为50.0g | F的质量为51.1g |
分析 根据浓硫酸、碱石灰的性质方面判断实验过程中的相关方面的问题,根据具体的数据可以进行相关方面的计算,从而得出正确的结论.
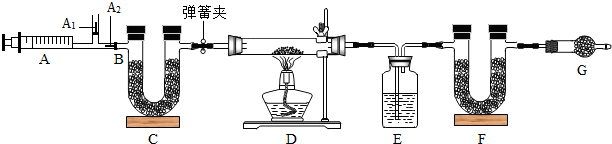
解答 解:(1)E装置的作用是吸收水蒸气,浓硫酸能吸收水蒸气,所以,E中的药品为浓硫酸.
(2)由于空气中含有二氧化碳和水蒸汽等,影响实验的结果,所以,C的作用是除去空气中的二氧化碳、水蒸气等气体杂质;F的作用是吸收生成的二氧化碳.G的作用:防止空气中的二氧化碳和水蒸气等杂质气体进入到F中,影响二氧化碳质量的测定.
(3)如果颠倒顺序,测量结果会偏高,故不能颠倒;若不进行步骤⑤的操作,生成的二氧化碳和水不能被充分吸收,使得结果偏小;该操作中推注射器时缓缓的目的是:使生成的二氧化碳、水蒸气吸收充分.
(4)根据表中的数据可知,反应后生成二氧化碳的质量为51.1g-50g=1.1g,
设碳酸氢钠的质量为x,分解生成的水的质量为y,根据化学方程式
2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O
168 44 18
x 1.1g y
$\frac{168}{x}=\frac{44}{1.1g}=\frac{18}{y}$解得:x=4.2g,y=0.45g;
故天然碱中含有结晶水的质量为102.25g-100.0g-0.45g=1.8g
天然碱中含有碳酸钠的质量为:16.6g-4.2g-1.8g=10.6g
根据天然碱的组成可知:$\frac{106a}{10.6}:\frac{84b}{4.2}:\frac{18c}{1.8}$ 所以a:b:c=2:1:2.
故答为:(1)浓硫酸,吸收水蒸气;
(2)除去空气中的二氧化碳、水蒸气等杂质气体; 吸收二氧化碳; 防止空气中的二氧化碳和水蒸气等杂质气体进入到F中,影响二氧化碳质量的测定;
(3)不能;偏小; 使生成的二氧化碳、水蒸气吸收充分;
(4)1.8; 2:1:2
点评 能够熟练的运用质量守恒定律以及化依据学方程式进行的相关计算,要充分理解物质的性质和实验目的,只有这样才能对问题做出正确的判断.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:填空题
 如图是A、B、C三种物质的溶解度曲线,看图回答下列问题:
如图是A、B、C三种物质的溶解度曲线,看图回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 课外兴趣小组对碳还原氧化铜的实验进行了如下创新探究:取一根洁净的石墨棒,置于一张大小适宜的铝箔内,在其表面均匀撤上适量氧化铜粉末,将其包紧,置于酒精灯火焰上加热(如图).几分钟后,冷却,发现氧化铜由黑色变为红色.
课外兴趣小组对碳还原氧化铜的实验进行了如下创新探究:取一根洁净的石墨棒,置于一张大小适宜的铝箔内,在其表面均匀撤上适量氧化铜粉末,将其包紧,置于酒精灯火焰上加热(如图).几分钟后,冷却,发现氧化铜由黑色变为红色.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 燃气灶能效标准将于2015年4月1日正式实施,这标志着与市民生活息息相关的燃气灶将进入节能时代,如图是一款燃气灶的示意图:
燃气灶能效标准将于2015年4月1日正式实施,这标志着与市民生活息息相关的燃气灶将进入节能时代,如图是一款燃气灶的示意图:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
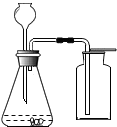 如图是实验室制取CO2的装置,请你回答:
如图是实验室制取CO2的装置,请你回答:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物 质 | 选用试剂(过量) | 操作方法 | |
| A | CO2(HCl) | 氢氧化钠溶液 | 通入装有氢氧化钠溶液的洗气瓶 |
| B | Cu(Fe) | 稀盐酸 | 加入稀盐酸充分反应后过滤、洗涤 |
| C | CuSO4溶液(H2SO4) | 氯化铜 | 加入氯化铜粉末充分反应后过滤 |
| D | 盐酸(H2SO4) | 硝酸钡溶液 | 加入硝酸钡溶液充分反应后过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com