
 五•一期间某同学从华蓥山上采集到一种石灰石,为了测定石灰石中CaCO3的含量.该同学取40克石灰石样品进行煅烧实验(所含杂质在煅烧过程中不发生变化,已知CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ ),测得反应后固体的质量(m)与反应时间(t)的关系如下表:
五•一期间某同学从华蓥山上采集到一种石灰石,为了测定石灰石中CaCO3的含量.该同学取40克石灰石样品进行煅烧实验(所含杂质在煅烧过程中不发生变化,已知CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ ),测得反应后固体的质量(m)与反应时间(t)的关系如下表:| 反应时间t∕s | t0 | t1 | t2 | t3 | t4 | t5 | t6 |
| 反应后固体的质量m∕g | 40 | 37.5 | 35 | 32.5 | 31 | 29 | 29 |
分析 根据图可以知道加热至固体质量不变时碳酸钙已经完全分解,可以确定碳酸钙完全分解的时间,根据质量守恒定律可知,过程中质量的减少是因为生成了二氧化碳,所以可以求算二氧化碳的质量,根据二氧化碳和对应的化学方程式求算碳酸钙的质量,最后根据对应的每个时间的固体减少量也就是生成的气体量画出曲线图.
解答 解:
由表可以看出,当加热到 t5时,固体质量不再减少,也就是CaCO3已经完全分解;
当固体不再减少时,根据质量守恒定律可知,生成的二氧化碳的质量也就是固体的减少量,为40g-29g=11g
设生成11g二氧化碳消耗的碳酸钙的质量为x
CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑
100 44
x 11g
$\frac{100}{44}$=$\frac{x}{11g}$
x=25g
处理数据得表
| 反应时间t∕s | t0 | t1 | t2 | t3 | t4 | t5 | t6 |
| 反应后固体的质量m∕g | 40 | 37.5 | 35 | 32.5 | 31 | 29 | 29 |
| 固体减少量也就是二氧化碳的质量 | 0 | 2.5 | 5 | 7.5 | 9 | 11 | 11 |


点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.


 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案科目:初中化学 来源: 题型:计算题
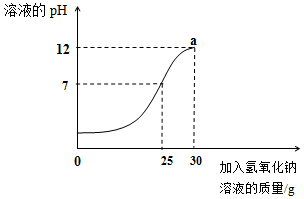 为测定某未知浓度的氢氧化钠溶液的溶质质量分数,取19.6%的稀硫酸溶液20g,逐滴加入氢氧化钠溶液30g,同时用pH计测定并记录反应过程中混合溶液pH变化情况(如图所示).请回答下列问题.
为测定某未知浓度的氢氧化钠溶液的溶质质量分数,取19.6%的稀硫酸溶液20g,逐滴加入氢氧化钠溶液30g,同时用pH计测定并记录反应过程中混合溶液pH变化情况(如图所示).请回答下列问题.查看答案和解析>>
科目:初中化学 来源: 题型:推断题
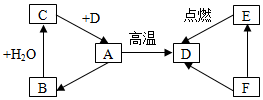
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 缺碘可能会导致人体的甲状腺肿大 | |
| B. | 可用甲醛溶液浸泡水产品防腐 | |
| C. | 老年人缺钙会发生骨质疏松,容易骨折 | |
| D. | 尿素[CO(NH2)2]是一种化学肥料,含有氮元素,它属于氮肥 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
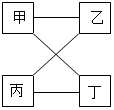 如表提供的四组物质,相连接的物质间在一定条件下可以发生,不相连接的物质间不能发生反应(即甲与丙、乙与丁不能发生反应).图示中符合题意要求的一组是( )
如表提供的四组物质,相连接的物质间在一定条件下可以发生,不相连接的物质间不能发生反应(即甲与丙、乙与丁不能发生反应).图示中符合题意要求的一组是( )| 甲 | 乙 | 丙 | 丁 | |
| A | Na2CO3 | Ca(OH)2 | HCl | CaCl2 |
| B | Mg | HCl | CuSO4 | NaOH |
| C | KOH | CO2 | NaOH | CuSO4 |
| D | CO | O2 | H2SO4 | CuO |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
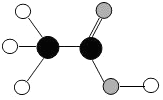 食醋是厨房中常用的调味品,它的主要成分是乙酸,乙酸分子的模型如图所示,其中
食醋是厨房中常用的调味品,它的主要成分是乙酸,乙酸分子的模型如图所示,其中 代表一个碳原子,
代表一个碳原子, 代表一个氢原子,
代表一个氢原子, 代表一个氧原子,下列说法不正确的是( )
代表一个氧原子,下列说法不正确的是( )| A. | 乙酸的化学式CH3COOH | |
| B. | 乙酸的相对分子质量为60 | |
| C. | 乙酸中碳元素的质量分数为60% | |
| D. | 乙酸分子中的碳原子、氢原子、氧原子的个数比为1:2:1 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | NaCl+KNO3═NaNO3+KCl | B. | 2Fe+6HCl═2FeCl3+3H2↑ | ||
| C. | Ca(OH)2+BaCO3═CaCO3↓+Ba(OH)2 | D. | Cu(OH)2+2HCl═CuCl2+2H2O |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 将草木灰(含K2CO3)与氯化铵混合施用 | |
| B. | 纯碱既可从内陆盐湖提取,又可用“侯氏联合制碱法”生产 | |
| C. | 用石灰乳与硫酸铜溶液混合配制防治植物病害的波尔多液 | |
| D. | 汽车或电动车的蓄电池中用到的硫酸溶液是由浓硫酸稀释而成 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com