

分析 (1)根据实验室常用仪器的名称进行分析;
(2)根据氯酸钾在二氧化锰的催化作用下,受热分解生成氯化钾和氧气,氧气的密度比空气的密度大,不易溶于水进行解答;
(3)根据制取硫化氢气体的反应原理解答;根据药品的状态和反应条件来决定制取硫化氢气体的发生装置的选择;
(4)根据检查装置气密性的方法分析解答.
解答 解:(1)图中标号①仪器的名称是集气瓶;
(2)实验室用加热氯酸钾和二氧化锰混合物制取氧气,氯酸钾在二氧化锰的催化作用下,受热分解生成氯化钾和氧气,反应的化学方程式为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;
氧气的密度比空气的密度大,不易溶于水,故收集氧气可选择D或E;实验室用氯酸钾和二氧化锰的混合物制氧气用固体加热装置,氧气不易溶于水、密度比空气大,氧气具有助燃性,能支持燃烧,能使带火星的木条复燃,所以用向上排空气法收集氧气验满方法:将带火星的木条放在集气瓶口,如果复燃,说明收集满了.
(3)硫化亚铁(FeS)固体和稀硫酸在常温下发生复分解反应制取硫化氢(H2S)气体,还会产生硫酸亚铁,故反应的方程式为:FeS+H2SO4═FeSO4+H2S↑;实验室通常用块状固体硫化亚铁(FeS)与稀硫酸在常温下反应制取硫化氢气体,故发生装置选择固液常温型装置,故选B或C;
(4)制取气体前应先检查装置的气密性,若按F图所示操作,结果在导管口未看到气泡,其可能原因与下列因素无关的是:将烧杯换成水槽;导管深入水中位置过深,气体无法逸出;将水换成冰水无关;检验时应先将导管放入水中,再用手捂住试管壁,故④有关.
故答案为:(1)集气瓶;(2)2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;D或E;(3)FeS+H2SO4═FeSO4+H2S↑;B或C;(4)①②③.
点评 本考点主要考查了气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.


 53随堂测系列答案
53随堂测系列答案科目:初中化学 来源: 题型:计算题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
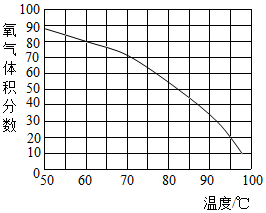 小亮发现:收集的氧气占集气瓶容积的60%(空气占40%)时,能使带火星的木条复燃.那么,使带火星的木条复燃的氧气浓度的最低值是多少呢?小亮对此展开探究:
小亮发现:收集的氧气占集气瓶容积的60%(空气占40%)时,能使带火星的木条复燃.那么,使带火星的木条复燃的氧气浓度的最低值是多少呢?小亮对此展开探究:| 第一组 | 第二组 | 第三组 | |||||||||
| 集气瓶编号 | ① | ② | ③ | ④ | ⑤ | ① | ② | ③ | ④ | ⑤ | ① |
| 收集的O2占容积的体积分数(%) | l0 | 20 | 30 | 40 | 50 | 3l | 33 | 35 | 37 | 39 | 34 |
| 带火星木条的状况 | 微亮 | 亮 | 很亮 | 复燃 | 复燃 | 很亮 | 很亮 | 复燃 | 复燃 | 复燃 | 很亮 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
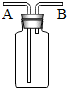 如图所示装置有多种用途,请回答下列问题:
如图所示装置有多种用途,请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Fe$→_{点燃}^{O_{2}}$Fe2O3$\stackrel{盐酸}{→}$FeCl3 | B. | SO2$\stackrel{H_{2}O}{→}$H2SO3$\stackrel{O_{2}}{→}$H2SO4 | ||
| C. | Na2CO3$\stackrel{Ca(NO_{3})_{2}}{→}$NaNO3$\stackrel{KCI}{→}$KNO3 | D. | CaCl2溶液$\stackrel{CO_{2}}{→}$CaCO3$\stackrel{NaOH}{→}$Ca(OH)2 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 次数 | 实验前 | 第1次 | 第2次 |
| 加入稀盐酸的质量/g | 0 | 50 | 50 |
| 剩余固体的质量/g | 5 | 3 | 2 |
| A. | 第 1 次加入稀盐酸后剩余固体中还有镁 | |
| B. | 第 2 次所加入的稀盐酸未反应完 | |
| C. | 每 50 g 稀盐酸和 1 g 镁恰好完全反应 | |
| D. | 合金样品中铜的质量分数为 40% |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
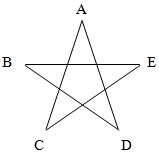 A、B、C、D、E五种物质均为初中化学中常见的化合物,它们之间的关系如右图所示,相互之间连线表示两者间能发生化学反应.A、C、E均为氧化物,A是人体呼出气体的主要成分;在实验室中B能用来制取A;C和E反应能生成D.请回答:
A、B、C、D、E五种物质均为初中化学中常见的化合物,它们之间的关系如右图所示,相互之间连线表示两者间能发生化学反应.A、C、E均为氧化物,A是人体呼出气体的主要成分;在实验室中B能用来制取A;C和E反应能生成D.请回答:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com