
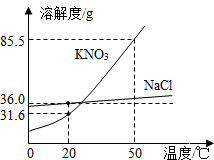
 NaCl、KNO3两种固体物质的溶解度曲线如图所示,下列说法正确的是( )
NaCl、KNO3两种固体物质的溶解度曲线如图所示,下列说法正确的是( )| A. | 20°C时,NaCl的溶解度为31.6g | |
| B. | KNO3的溶解度大于NaCl的溶解度 | |
| C. | 使NaCl从其饱和溶液中析出,可采用蒸发溶剂的方法 | |
| D. | 50℃时,在100g水中加入100gKNO3,所得溶液中KNO3的质量分数为50% |
分析 根据题目信息和溶解度曲线可知:硝酸钾、氯化钠两种固体物质的溶解度,都是随温度升高而增大,而硝酸钾的溶解度随温度的升高变化比氯化钠大;20°C时,NaCl的溶解度为36g,不是31.6g;KNO3的溶解度大于NaCl的溶解度错误,因为没有指明温度;使NaCl从其饱和溶液中析出,可采用蒸发溶剂的方法正确,因为水分蒸发,有固体析出;50℃时,硝酸钾的溶解度是85.5g,因此在100g水中加入100gKNO3,所得溶液中KNO3的质量分数=$\frac{85.5g}{185.5g}×100%$≈46.1%,50%是错误的.
解答 解:A、20°C时,NaCl的溶解度为36g,不是31.6g,故选项错误;
B、KNO3的溶解度大于NaCl的溶解度错误,因为没有指明温度,故选项错误;
C、使NaCl从其饱和溶液中析出,可采用蒸发溶剂的方法正确,因为水分蒸发,有固体析出;故选项正确;
D、50℃时,硝酸钾的溶解度是85.5g,因此在100g水中加入100gKNO3,所得溶液中KNO3的质量分数=$\frac{85.5g}{185.5g}×100%$≈46.1%,50%是错误的,故选项错误;
故选C
点评 本考点考查了溶解度曲线及其应用,通过溶解度曲线我们可以获得很多信息;还考查了有关溶液和溶质质量分数的计算,有关的计算要准确,本考点主要出现在选择题和填空题中.


 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案科目:初中化学 来源: 题型:选择题
| A. | ②③⑥⑧ | B. | ②⑤⑥⑧ | C. | ①③④⑧ | D. | ①④⑥⑦ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 主食 | 米饭 馒头 |
| 副食 | 红烧肉 鸡蛋 豆腐汤 |
| 饮料 | 纯净水 可乐 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 制取成本高和贮存困难 | B. | 氢气燃烧条件难以满足 | ||
| C. | 制备氢气原料极其匮乏 | D. | 氢气燃烧过程难以控制 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 通过化学启蒙学习,同学们对组成万物的基本物质有了进一步了解.
通过化学启蒙学习,同学们对组成万物的基本物质有了进一步了解.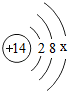 ,其中x=4.
,其中x=4.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
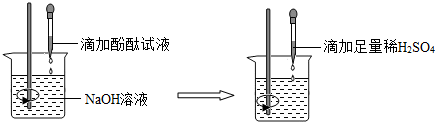
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
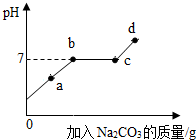 烧杯中盛有CaCl2和HCl的混合溶液,向其中滴加Na2CO3溶液,烧杯中溶液的pH与滴加溶液的质量关系如图所示.下列说法错误的是( )
烧杯中盛有CaCl2和HCl的混合溶液,向其中滴加Na2CO3溶液,烧杯中溶液的pH与滴加溶液的质量关系如图所示.下列说法错误的是( )| A. | a点的溶质为HCl、NaCl | |
| B. | ab段反应产生大量气泡 | |
| C. | bc段反应的方程式为CaCl2+Na2CO3═2NaCl+CaCO3↓ | |
| D. | 取d点溶液滴加酚酞试液,溶液显红色 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | X>Z>Y | B. | X>Y>Z | C. | Y>Z>X | D. | Z>Y>X |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com