
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:选择题
| A. | 木炭在空气中燃烧时,发出白光,生成二氧化碳气体 | |
| B. | 水通电时,正极产生的气体是氢气 | |
| C. | 灼烧羊毛有烧焦羽毛的气味 | |
| D. | 打开浓盐酸瓶盖,瓶口会冒白烟 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
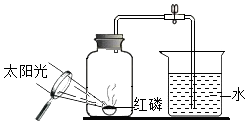 用来测定空气成分的方法很多,如图所示的是用红磷在空气中燃烧的测定方法.
用来测定空气成分的方法很多,如图所示的是用红磷在空气中燃烧的测定方法.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
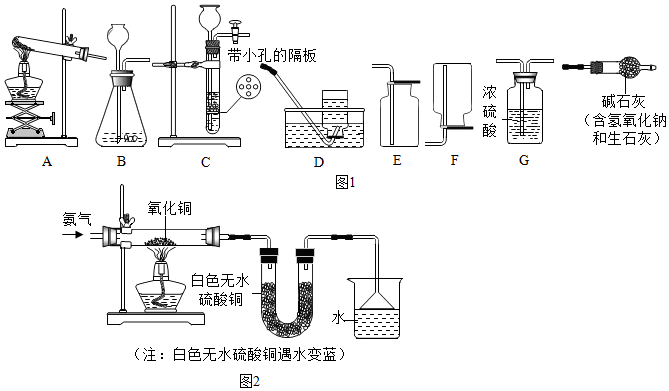
| 步骤 | 现象 | 结论 |
| 红色物质中有 Cu2O |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
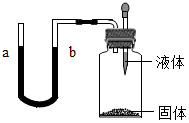 如图密闭实验装置,能使液面a比液面b高,过一段时间又回到持平的一组固体和液体可以是( )
如图密闭实验装置,能使液面a比液面b高,过一段时间又回到持平的一组固体和液体可以是( )| A. | 食盐和水 | B. | 锌和硫酸 | ||
| C. | 固体氢氧化钠和水 | D. | 硝酸铵和水 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
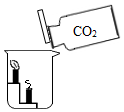 在探究二氧化碳性质时如图所示实验
在探究二氧化碳性质时如图所示实验查看答案和解析>>
科目:初中化学 来源: 题型:解答题
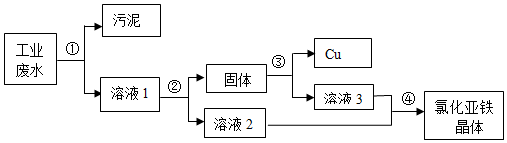
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | C→CO2→CO | B. | Fe2O3→Fe2(SO4)3→Fe(OH)3 | ||
| C. | NaCl→NaNO3→NaOH | D. | SO3→Na2SO4→BaSO4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com