
已知氢氧化锂(LiOH)可溶于水,其化学性质与氢氧化钠相似。下列对氢氧化锂的化学性质的说法中错误的是( )
A. 能与二氧化碳反应
B. 能使无色酚酞试液变红
C. 能与稀硫酸反应
D. 能使紫色石蕊试液变红
D 【解析】氢氧化锂和氢氧化钠的化学性质相似,能和二氧化碳反应生成盐和水;其溶液呈碱性,能使酚酞溶液变红,能使紫色石蕊溶液变蓝,能和酸发生中和反应,故选D.科目:初中化学 来源:上海市徐汇区2018届中考二模化学试卷 题型:单选题
在硝酸银和硝酸铜的混合溶液中,加入一定量的铁粉,充分反应后,有少量金属析出,过滤后,向滤液中滴加稀盐酸,有白色沉淀析出,则析出的少量金属是
A. 铜 B. 银 C. 铁和铜 D. 铜和银
B 【解析】金属活动性顺序中,排在前面的金属能把排在后面的金属从其化合物的水溶液中置换出来,金属活动性差距越大,越易发生化学反应,所以首先发生的化学反应是:Fe+2AgNO3=2Ag+ Fe(NO3)2 ,当硝酸银溶液完全反应后,铁粉才与硝酸铜溶液反应,Fe+Cu(NO3)2==Fe(NO3)2+Cu。 向滤液中滴加稀盐酸,有白色沉淀析出,说明滤液中含有AgNO3溶液,则铁粉无剩余,铁...查看答案和解析>>
科目:初中化学 来源:黑龙江省大庆市杜尔伯特县2018届九年级(初四)下学期期中考试化学试卷 题型:综合题
我国的瓷器举世闻名,普通陶瓷中含有铝元素,其元素符号为_________,该元素氧化物的化学式为__________(并请标出其中铝元素的化合价)。普通玻璃中含有钠元素,含该元素碱的化学式为__________,常温下其溶液的pH_____7(填:“>”、“=”、“<”),若向其溶液中加水,则所得溶液的pH_________(填:“增大”、“减小”、“不变”)。陶瓷和玻璃的主要成分都是硅酸盐,它们同属于__________材料(填字母)。A. 金属 B. 无机非金属 C. 合成 D. 复合
Al Al2O3 NaOH > 降低 B 【解析】由题意可知:铝元素的元素符号Al,其氧化物化学式为Al2O3,由钠元素组成的碱中一定含氢氧根离子,故其化学式应为:NaOH,其水溶液显碱性PH>7,若向其溶液中加水,溶质质量分数减小,碱性减弱,则所得溶液pH降低。陶瓷和玻璃的主要成分都是硅酸盐,它们同属于无机非金属材料。查看答案和解析>>
科目:初中化学 来源:江苏省宿迁市2018届九年级下学期阶段性检测化学试卷 题型:科学探究题
某研究小组对自动充气气球(示意图如图1)进行下列探究.
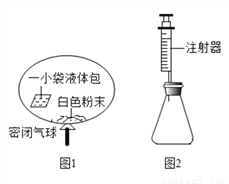
【查阅资料】该气球充气原理是:通过挤破液体包,使液体与白色粉末接触产生二氧化碳气体,实现气球自动充气.
(1)为了检验气体是二氧化碳,可选用____(填试剂名称),反应方程式为_______________。
探究一:液体包内溶液酸碱性的探究
(2)室温时,用pH试纸测得溶液的pH=3,则该溶液呈_____性。
探究二:白色粉末成分的探究
【猜想与假设】
甲同学认为是碳酸钙; 乙同学认为是碳酸钠; 丙同学认为是碳酸氢钠。
【设计并进行实验】
(3)将少量白色粉末放入水中搅拌,固体全部溶解,说明________同学的猜想不正确。
(4)室温时,分别向盛有碳酸氢钠、碳酸钠和白色粉末样品的锥形瓶中注入等体积、足量的10%盐酸(装置如图2),记录如表:
实验编号 | 锥形瓶内物质 | 最终得到CO2体积/mL | |
名称 | 质量/g | ||
① | 碳酸氢钠 | 5 | V1 |
② | 碳酸钠 | 5 | V2 |
③ | 白色粉末 | x | V1 |
实验①的化学方程式为__________;表中x=_____;V1 ____V2(填“>”、“<”或“=”)。
【分析并得出结论】:
(5)白色粉末是_________。
澄清石灰水 Ca(OH)2 + CO2 = CaCO3↓+ 2H2O 酸 甲 NaHCO3 + HCl = NaCl +H2O +CO2↑ 5 > 碳酸氢钠 【解析】(1)为了检验气体是二氧化碳,可选用澄清石灰水,二氧化碳可使石灰水变浑浊,反应方程式为Ca(OH)2 + CO2 = CaCO3↓+ 2H2O。探究一:液体包内溶液酸碱性的探究。(2)室温时,用pH试纸测得溶液的pH=3,则该溶...查看答案和解析>>
科目:初中化学 来源:江苏省宿迁市2018届九年级下学期阶段性检测化学试卷 题型:单选题
下列物质不能用来验证烧碱溶液和稀盐酸是否发生反应的是( )
A. 酚酞试液 B. 镁条 C. 硝酸银溶液 D. 硫酸铜溶液
C 【解析】烧碱溶液和稀盐酸反应属于无明显现象的中和反应。A、酚酞试液遇酸不变色,遇碱变红色;B、镁条与稀盐酸反应产生氢气;C、硝酸银溶液与氯离子反应生成氯化银白色沉淀,烧碱溶液和稀盐酸反应后生成氯化钠,也含有氯离子;D、硫酸铜溶液与烧碱溶液反应生成氢氧化铜蓝色沉淀。故不能用来验证烧碱溶液和稀盐酸是否发生反应的是C。 点睛∶对于没有明显现象的中化合反应,可以使用指示剂石蕊或酚酞,可以使...查看答案和解析>>
科目:初中化学 来源:江苏省宿迁市2018届九年级下学期阶段性检测化学试卷 题型:单选题
下列物质露置于空气中,因发生化学变化而使质量增加的是( )
A. 浓硫酸 B. 烧碱溶液 C. 浓盐酸 D. 过氧化氢溶液
B 【解析】A、浓硫酸具有吸水性,属于因发生物理变化而使质量增加;B、烧碱溶液与二氧化碳反应生成碳酸钠溶液,属于因发生化学变化而使质量增加;C、浓盐酸具有挥发性,属于属于因发生物理变化而使质量减小;D、过氧化氢溶液,属于属于因发生物理变化而使质量减小。故选B。 点睛∶浓硫酸具有吸水性,浓盐酸具有挥发性均属于物理性质。查看答案和解析>>
科目:初中化学 来源:江苏省常熟市2018届九年级下学期适应性质量检测化学试卷 题型:科学探究题
化学兴趣小组为验证质量守恒定律,做了镁条在空气中然烧的实验(如图1)。

同学们观察到镁条在空气中剧烈燃烧,发出耀眼的白光,因此镁在军事上作_________;
同时同学们还观察到产生的大量白烟弥漫到空气中,最后一些白色固体掉落在仪器A上。
(1)上述仪器A名称是____________。
(2)同学们通过称量发现:在仪器A上收集到产物的质量小于镁条的质量。有人认为这个反应不遵循质量守恒定律。你认为出现这样实验结果的原因可能是:____________。
(3)小红按下图2装置改进实验,验证了质量守恒定律,还发现产物中有少量黄色固体。
【提出问题】黄色固体是什么?
【查阅资料】①氧化镁为白色固体;②镁能与氮气剧烈反应生成黄色的氮化镁( Mg3N2)固体;③氮化镁可与水剧烈反应产生氨气,该气体能使湿润的红色石蕊试纸变蓝。
【做出猜想】黄色固体是Mg3N2
【实验探究】请设计实验,验证猜想
实验操作 | 实验现象及结论 |
_______________________ | ________________ |
【反思与交流】
①写出镁条燃烧生成氮化镁的化学方程式为____________________;
②空气中N2的含量远大于O2的含量,可是镁条在空气中燃烧产物MgO却远多于Mg3N2,合理的解释是:_________________;
③同学们又联想到氢气在氯气中能够燃烧,于是对燃烧条件又有了新的认识:___________
照明弹、信号弹、闪光弹、诱饵弹等 石棉网 反应生成的氧化镁部分扩散到空气中 取适量黄色固体样品于试管中,向试管中加入适量水,在试管口放湿润的红色石蕊试纸 湿润的红色石蕊试纸变蓝色,说明黄色固体是氮化镁 3Mg+N22Mg3N2 相同条件下,氧气比氮气更容易和镁反应 燃烧不一定需要氧气 【解析】镁条燃烧生成氧化镁,反应的化学方程式为:2Mg+O22MgO,因此镁在军事上作照明弹、信号弹、闪...查看答案和解析>>
科目:初中化学 来源:江苏省常熟市2018届九年级下学期适应性质量检测化学试卷 题型:单选题
碘盐中通常含有少量的碘酸钾(化学式为KIO3) ,下列说法正确的是
A. 碘酸钾中碘元素质量分数最大
B. 在家里可以用碘盐来检验淀粉
C. 碘酸钾中钾、碘、氧元素质量比为1:1:3
D. 碘酸钾中碘元素的化合价为―1价
A 【解析】A、根据碘酸钾(KIO3)的化学式可知,各元素的质量比K:I:O=39:127:48,故碘酸钾中碘元素质量分数最大,正确;B、碘盐中碘的含量很低,故不能用来检验淀粉,错误;C、根据碘酸钾(KIO3)的化学式可知,各元素的质量比K:I:O=39:127:48;错误;D、碘酸钾中钾元素为+1价,氧元素为?2价,根据化合物中正负化合价的代数和为0,设碘元素的化合价为x,则+1+x+(?...查看答案和解析>>
科目:初中化学 来源:安徽省合肥市育英学校2018届九年级中考模拟化学试卷 题型:单选题
下列操作能达到实验目的的是:
A. 可用燃着的木条来区别氮气、氧气和二氧化碳
B. 用稀硫酸除去氯化钠溶液中含有的少量碳酸钠
C. 通过盛浓硫酸的洗气瓶除去氧气中的水蒸气
D. 加入铁粉除去硫酸锌溶液中含有的少量硫酸
C 【解析】A、氮气和二氧化碳都不会助燃,将燃着的木条伸入氮气和二氧化碳中的都熄灭现象相同,故A错误; B、碳酸钠会和硫酸反应生成硫酸钠,虽然除去了碳酸钠,但硫酸钠对氯化钠来说也是杂质,没有达到除杂的目的,故B错误; C、浓硫酸有吸水性,能够吸收氧气中的水蒸气,故C正确; D、铁会和硫酸反应生成硫酸亚铁,没有除去硫酸锌而除去了铁,故D错误。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com