
我国古代典籍中有”银针验毒”的记载,“银针验毒”的反应原理之一是
4Ag+2H2S +O2=2X+2H2O。下列有关该反应的说法不正确的是
A. 反应属于氧化反应 B. X的化学式是Ag2S
C. 反应前后元素的种类不变 D. 反应前后所有元素的化合价都发生了变化
D 【解析】A.反应属于氧化反应。故A正确。根据质量守恒定律知,B.X的化学式是Ag2S。故B正确。C.反应前后元素的种类不变。故C正确。D.反应前后只有银,硫元素的化合价发生了变化。故D错误。 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源:江苏省苏州市高新区2018届九年级上学期期末考试化学试卷 题型:填空题
下列关于物质性质及用途的说法是否正确?正确的在括号中打“√”,错误的打“x”。
(1)稀有气体通电时发出不同颜色可以用作霓虹灯电光源。________
(2)金属钨具有极高熔点,常用作电池的电极。________
(3)酒精是一种溶剂,可以用于溶解中草药中的有效成分。________
(4)液氧具有助燃性,可用作火箭发射的助燃剂。________
(5)甲烷燃烧放出热量可用于高温切割和焊接金属。________
√ ? √ √ ? 【解析】(1)稀有气体通电时发出不同颜色可以用作霓虹灯电光源,正确;(2)金属钨具有极高熔点,常用作灯丝,错误;(3)酒精是一种溶剂,可以用于溶解中草药中的有效成分,正确;(4)液氧具有助燃性,可用作火箭发射的助燃剂,正确;(5)乙炔燃烧放出热量可用于高温切割和焊接金属,错误。查看答案和解析>>
科目:初中化学 来源:广东省东莞市堂星晨学校2018届考第一次模拟化学试卷 题型:填空题
缺铁性贫血中的“铁”是指 ____(填“铁元素”、“铁原子”或“单质铁”)。某补铁剂主要成分是富马酸亚铁(C4H2FeO4),它由_____种元素组成,其中_____ 元素的质量分数最高,C、H元素的原子个数比为____。1mol C4H2FeO4中约含有____个氢原子。
铁元素 4 氧 2:1 1.204×1024 【解析】元素属于宏观概念,只讲种类,不讲个数。缺铁性贫血中的“铁”是指铁元素。某补铁剂主要成分是富马酸亚铁(C4H2FeO4),它由碳,氢,铁,氧四种元素组成,其质量比是12×4∶2∶56∶16×4=24∶1∶28∶32,其中氧元素的质量分数最高,C、H元素的原子个数比为4∶2=2:1。1mol C4H2FeO4中约含有2×6.02×1023 =...查看答案和解析>>
科目:初中化学 来源:江苏省东台市2017-2018学年度第二学期九年级化学综合试卷检测卷 题型:综合题
实验窒常会产生含硫酸的废水,需经处理至中性。某兴趣小组同学配制一定质量分数的氢氧化钾溶液来处理酸性废水。
(1)定性检测废水
检测废水呈酸性的方法是_____________。
(2)配制200 g质量分数为5.6%的氢氧化钾溶液
①计算
m (KOH)=_______g,V(H2O)=________mL(水的密度近似为1.0 g·mL-1)。
②称取氢氧化钾
调节托盘天平平衡后,将一只烧杯放在托盘天平的左盘,称量其质量。然后______(按操作先后顺序,填字母),直至天平平衡。
A.向烧杯中加氢氧化钾同体 B.按需要添加砝码、移动游码
③量取水;④溶解;⑤转移。
(3)定量测定废水
取酸性废水样品100 g,逐滴加入5.6%的氢氧化钾溶液,废水中硫酸的质量分数变化如右下图所示。(假设废水中其他成分不与氢氧化钾反应且不含硫酸钾)

①P点对应溶液中一定存在的阳离子有_______(填离子符号)。
②酸性废水中硫酸的质量分数为______(用百分数表示,保留到0.1%)。
③计算当废水处理至中性时,溶液中硫酸钾的质量分数(写出计算过程,结果用百分数表示,保留到0.l%)。
(1)取样,滴人紫色石蕊试液,若变红则呈酸性(或其他合理答案) (2)①11.2 188.8 ②BA (3)①K+、H+ ②4.9% ③4.4% 【解析】(1)检验溶液的酸碱性可用酸碱指示剂。废水中含有硫酸,那么可用紫色石蕊试液,方法是:取样,滴人紫色石蕊试液,若变红则呈酸性; (2)①配制200 g质量分数为5.6%的氢氧化钾溶液, 需要的溶质氢氧化钾的质量=200...查看答案和解析>>
科目:初中化学 来源:江苏省东台市2017-2018学年度第二学期九年级化学综合试卷检测卷 题型:单选题
金属钴(Co)与铁的化学性质相似,都能与稀盐酸反应,在化合物中钻元素常显+2、+3价,下列说法正确的是( )
A. CoCl3读作“氯化亚钴
B. CoCl3中钴元素的化合价为+2价
C. 金属铜不能与CoCl2溶液发生反应
D. CoCl2中钻元素的质量分数约为33.3%
C 【解析】A、CoCl3读作“氯化钴”,错误;B、CoCl3中氯元素的化合价为﹣1价,则钴元素的化合价为+3价,错误;C、金属钴(Co)与铁具有相似的化学性质,能够和盐酸反应,说明Co位于氢前,因此Co的活动性比铜强,故铜不能和CoCl2溶液发生反应;正确;D、CoCl2中钴元素的质量分数=×100%≠33.3%,错误。故...查看答案和解析>>
科目:初中化学 来源:江苏省东台市2017-2018学年度第二学期九年级化学综合试卷检测卷 题型:单选题
下列过程中利用了物质的化学性质的是
A. 液氮作制冷剂 B. 乙炔与氧气形成高温氧炔焰
C. 酒精洗掉沾在试管壁上的碘 D. 洗洁精通过乳化作用除去油污
B 【解析】化学性质是通过化学变化表现出来的性质,物理变化不需要化学变化就表现出来的性质;A选项液氮制冷剂,利用液氮变化为气态吸热为物理性质;B选项乙炔与氧气形成高温氧炔焰,发生了化学变化利用了化学性质;C选项酒精洗掉沽在试管壁上的碘 ,为酒精易溶于酒精,利用了物理性质;D选项洗洁精通过乳化作用除去油污,属于物质的物理性质;故答案选择B查看答案和解析>>
科目:初中化学 来源:黑龙江省2017届九年级下学期第一次月考化学试卷 题型:简答题
根据化学方程式C+O2 CO2 ,从物质种类、质量和反应条件等方面考虑,你能得到的信息有哪些?
CO2 ,从物质种类、质量和反应条件等方面考虑,你能得到的信息有哪些?
查看答案和解析>>
科目:初中化学 来源:黑龙江省2017届九年级下学期第一次月考化学试卷 题型:单选题
在一密闭容器内有氢气和氧气的混合气体10g,经点火后生成9g水。问原混合气体中氢气和氧气的质量比为 ( )
A. 3∶7 B. 1∶4 C. 4∶6 D. 1∶1
B 【解析】9g水中氢元素的质量为1g,氧元素的质量为8g ,故参加反应的氢气和氧气的质量为1g和8g,故有1个的气体剩余,当剩余气体是氢气时,氢气的质量为2g,故氢气和氧气的质量比为2:8=1:4,当剩余气体是氧气时,氢气与氧气的质量比为1:9,故选B。查看答案和解析>>
科目:初中化学 来源:江苏省泰兴市2018届九年级下学期第一次阶段测试化学试卷 题型:多选题
能正确反映对应变化关系的图像是
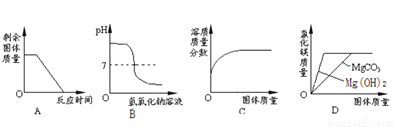
A. 高温煅烧一定质量的石灰石固体
B. 向一定量的稀硫酸中滴加氢氧化钠溶液至过量
C. 一定温度下,向不饱和硝酸钠溶液中不断加入硝酸钠固体,充分搅拌
D. 分别向同质量、同质量分数的稀盐酸中不断加入碳酸镁和氢氧化镁固体
CD 【解析】A、高温煅烧石灰石有固体氧化钙生成,故最终固体的质量不可能降为0,错误; B、向一定量的稀硫酸中滴加氢氧化钠溶液至过量,一开始,溶液的pH小于7,结束后pH大于7 ,错误; C、一定温度下,向不饱和硝酸钠溶液中不断加入硝酸钠固体,充分搅拌,刚开始,硝酸钠固体溶解,溶液中溶质的质量分数增加,当达到饱和状态,硝酸钠不再溶解,溶质的质量分数不变,正确; D、碳酸镁的...查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com