
【题目】NaOH在工业上具有广泛的应用,某研究性学习小组通过以下实验探究NaOH的性质。
实验一 向两块固体表面滴加稀盐酸 | 实验二 振荡2个塑料瓶 |
|
|
(1)实验一中滴加盐酸后产生的气泡的化学式为_______________。
(2)实验二中振荡2个塑料瓶,观察到塑料瓶变瘪的程度为A>B, A瓶出现沉淀,B瓶中先有白色沉淀,继续振荡后沉淀消失。
①请说出一-种鉴别NaOH固体和Ca(OH)2固体的物理方法:__________________。
②B瓶中产生沉淀的化学方程式为_________________。
(3)在20°C时,研究小组对A瓶中产生沉淀的原因及成分做了如下探究:
[提出问题]两只塑料瓶中发生了哪些反应,得到了哪些物质?
[查阅资料]①20°C时,有关物质的溶解度如下表所示:
物质 | NaOH | Ca(OH)2 | Na2CO3 | NaHCO3 | CaCO3 | Ca(HCO3)2 |
溶解度/g | 109 | 0.18 | 21.5 | 9.6 |
| 16.6 |
②CO2可以与Na2CO3溶液发生反应: ![]() 。
。
③NaHCO3固体在120°C开始分解: ![]() 。Na2CO3 加热不分解。
。Na2CO3 加热不分解。
④常温下,饱和Na2CO3溶液pH为12.3, 饱和NaHCO3溶液pH为8.1。
根据以上资料和实验现象推断:B瓶最终所得澄清溶液中所含溶质为____________。
[提出猜想]对A瓶中沉淀成分有以下四种猜想:猜想Ⅰ : NaOH和Na2CO3;
猜想Ⅱ: Na2CO3; 猜想Ⅲ: Na2CO3 和NaHCO3; 猜想Ⅳ: NaHCO3。
小组同学经过讨论分析后,认为“猜想I”不成立,其理由是___________________。
[实验探究]将A瓶固体过滤后,用冰水洗涤,在烘箱中烘干。烘箱温度应控制为_______________。
小组甲:取2g固体溶于98gH2O配成溶液,用pH试纸测得其pH约为11。则_______________(填“猜想Ⅱ”、“猜想Ⅲ”、“猜想Ⅳ”)不成立。.
小组乙:取干燥固体在硬质大试管中加热,并将导管通入装有澄清石灰水的烧杯中。加热过程中,一直未见烧杯中有沉淀产生;将试管中固体冷却后称量, 其质量__________(填“变大”“变小”或“不变”)。
[实验结论]____________(填“猜想Ⅱ”、“猜想Ⅲ”、“猜想Ⅳ”)是正确的。
[反思评价]若不进行实验操作,仅通过比较塑料瓶中气体和溶液中溶质质量的相对关系,也可推断出A瓶中所得产物种类,还需要查阅或测量的数据是_______________。
【答案】CO2 将等量固体放入盛有少量水的试管中,用手轻轻触碰试管外壁,如果发烫说明是氢氧化钠,如果不发烫,说明是氢氧化钙 ![]() 碳酸氢钙 随着反应的进行,氢氧化钠的质量逐渐减小,因此氢氧化钠不会析出 120℃以下 Ⅳ 不变 猜想Ⅱ 20℃时,二氧化碳气体的密度和氢氧化钠饱和溶液的密度
碳酸氢钙 随着反应的进行,氢氧化钠的质量逐渐减小,因此氢氧化钠不会析出 120℃以下 Ⅳ 不变 猜想Ⅱ 20℃时,二氧化碳气体的密度和氢氧化钠饱和溶液的密度
【解析】
(1)实验一中,氢氧化钠和空气中的二氧化碳反应生成了碳酸钠和水,滴加稀盐酸后,碳酸钠和稀盐酸反应生成氯化钠、二氧化碳和水,气泡为二氧化碳,化学式是CO2;
(2)①氢氧化钠溶液溶于水放热,氢氧化钙微溶于水,溶解量较小,温度变化不大,故鉴别NaOH固体和Ca(OH)2固体:可将等量固体放入盛有少量水的试管中,用手轻轻触碰试管外壁,如果发烫说明是氢氧化钠,如果不发烫,说明是氢氧化钙;
②B瓶中氢氧化钙和二氧化碳反应生成碳酸钙和水,该反应的化学方程式为:![]() ;
;
(3)④氢氧化钠和二氧化碳反应生成了碳酸钙和水,碳酸钙和水、二氧化碳反应生成了碳酸氢钙,碳酸氢钙易溶于水,故B瓶最终所得澄清溶液中所含溶质为碳酸氢钙;
提出猜想:猜想Ⅰ不成立的理由是:随着反应的进行,氢氧化钠的质量逐渐减小,因此氢氧化钠不会析出;
实验探究:烘箱温度应控制在120℃以下,因为碳酸氢钠在120℃时会分解;
小组甲:取2g固体溶于98gH2O配成溶液,用pH试纸测得其pH约为11,常温下,饱和Na2CO3溶液pH为12.3, 饱和NaHCO3溶液pH为8.1,故猜想Ⅳ不成立;
小组乙:取干燥固体在硬质大试管中加热,并将导管通入装有澄清石灰水的烧杯中。加热过程中,一直未见烧杯中有沉淀产生,烧杯中无沉淀产生,说明无二氧化碳生成,因为![]() ,碳酸钠加热不分解,因此,固体中不含碳酸氢钠,该固体应为碳酸钠,碳酸钠受热不分解,因此将试管中固体冷却后称量,其质量不变;
,碳酸钠加热不分解,因此,固体中不含碳酸氢钠,该固体应为碳酸钠,碳酸钠受热不分解,因此将试管中固体冷却后称量,其质量不变;
实验结论:由以上分析可知,猜想Ⅱ正确;
反思评价:仅通过比较塑料瓶中气体和溶液中溶质质量的相对关系,也可推断出A瓶中所得产物种类,还需要查阅或测量的数据是:20℃时,二氧化碳气体的密度和氢氧化钠饱和溶液的密度,根据二氧化碳的密度和体积可以得出二氧化碳的质量,根据氢氧化钠的密度和体积可以得出氢氧化钠的质量,根据化学方程式:![]() ,
,![]() ,就可以得出相关产物的质量,然后根据20℃时,各物质的溶解度,就可以推出产物种类。
,就可以得出相关产物的质量,然后根据20℃时,各物质的溶解度,就可以推出产物种类。


 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案科目:初中化学 来源: 题型:
【题目】下列说法中,符合质量守恒定律的是 ( )
A.电解8g水可得4g氢气和4g氧气B.6g的碳与6g氧气反应生成12g二氧化碳
C.8g氧气与1g氢气化合生成9g水D.6g氧气与2g碳反应生成8g二氧化碳
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下列图示的探究过程,回答问题:
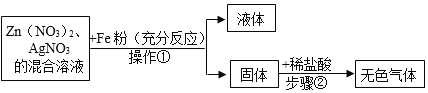
(1)操作①的名称_____,加入铁粉的化学方程式_____。
(2)图中固体中含有的物质(化学式)_____。
(3)写出步骤②发生反应的化学方程式_____。
(4)“液体”的成分中除了水外,还有_____(填化学式)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙、丙、丁是初中化学常见的四种物质,甲属于常见的酸,乙是相对分子质量最小的氧化物。它们相互之间的关系如图所示(“—”表示两种物质之间可以相互反应,“→”表示一种物质可生成另一种物质。)
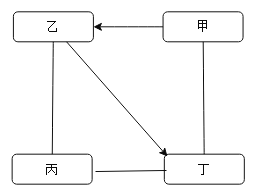
(1) 乙生成丁的化学方程式___________________________。
(2) 丙与丁反应的化学方程式__________________________。
(3) 甲与丁反应的微观实质为_________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是 A、B 两物质的溶解度曲线,下列信息中正确的是
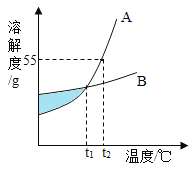
A. 图中阴影部分表明 A、B 两溶液都是饱和溶液
B. t1℃时,A、B 两饱和溶液的溶质质量分数相等
C. t2℃时,B 物质的溶解度大于 A 物质的溶解度
D. t2℃时,等质量的 A、B 两饱和溶液降温到 t1℃时析出溶质的质量相等
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】微波炉大大方便了人们的日常用餐。下图是某款微波炉的结构示意图,请回答。

(1)上述主要材料中属于合金的是____(只需写出一种, 下同);属于有机材料的是___。
(2)不锈钢机身可以避免生锈延长使用年限。工业上生锈的物品常可以用____(填名称)来除锈,若未能控制好时间,往往会看到有气泡产生,引起该现象的反应方程式是____。
(3)回收金属是保护有限金属资源的途径之一,请你写出一条回收金属的重要性____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】PX是“对二甲苯”(para-xylene)的英文缩写,化学式是C8H10。很多市民戴的口罩、穿的服装都是用PX做的。PX是无色透明有芳香气味的液体;有挥发性,但比汽油低;熔点13.2°C、沸点138.5°C;密度0.86g/cm3;可燃;低毒,毒性与汽油相当;遇火可爆炸,但爆炸性比汽油低。对于PX的说法正确的是( )
A.保存和储运PX应注意密封、禁止明火
B.根据物质的分类PX属于有机高分子化合物
C.PX完全燃烧时生成二氧化碳和水的分子个数比是4 :5
D.PX易溶于水
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】侯氏制碱法生产的碳酸钠中常含有少量的氯化钠。某学习小组对其组成展开探究。取碳酸钠和氯化钠的混合物样品24g,加入100g水使其完全溶解,再加入96g过量的氯化钙溶液,反应过程中生成沉淀的质量与氯化钙溶液的质量关系如图所示:
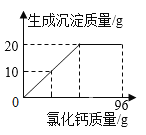
(1)完全反应时,得到的沉淀质量是_____g。
(2)计算样品中Na2CO3的质量分数_____。(写出计算过程,结果保留一位小数)。
(3)通过已知数据,可以求出的量有_____(写字母)。
A 反应后溶液的总质量
B 参加反应的氯化钙质量
C 氯化钙溶液中溶质的质量分数
D 恰好完全反应时,溶液中氯化钠的溶质质量分数
(4)取混合物样品24g,加入足量的稀盐酸,将生成的二氧化碳通入盛有8g炽热碳粉的密闭容器中充分反应,在下图中画出二氧化碳的质量与容器中固体质量变化的关系图_____。
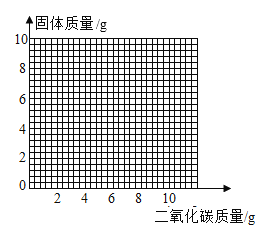
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是甲、乙两种固体物质在水中的溶解度曲线。下列说法不正确的是( )
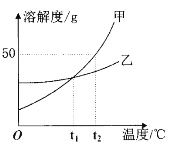
A. t1℃时,甲、乙两种物质的饱和溶液中溶质的质量分数相等
B. t2℃时,甲的饱和溶液中溶质的质量分数为50%
C. 质量相同的甲、乙饱和溶液,由t2℃降温到t1℃,甲比乙析出晶体的质量多
D. t2℃时,将20g甲物质加入50g水中,充分溶解后溶液的质量为70g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com