
 物质之间发生化学反应时常伴随有明显的现象,但有些化学反应却观察不到明显的现象.某班同学为证明NaOH能与稀盐酸发生中和反应,从不同角度设计了如下实验方案,并进行实验.
物质之间发生化学反应时常伴随有明显的现象,但有些化学反应却观察不到明显的现象.某班同学为证明NaOH能与稀盐酸发生中和反应,从不同角度设计了如下实验方案,并进行实验.分析 可以从物质和酸碱指示剂相互作用的显色情况方面和物质之间相互作用时的实验现象方面进行分析、考虑,从而得出正确的结论.
解答 解:【方案一】氢氧化钠能使酚酞变红色,所以可以再滴加氢氧化钠或者酚酞,观察颜色的变化,然后确定氢氧化钠和盐酸发生中和反应;
【方案二】显碱性的溶液稀释时溶液的pH越来越小,但是不能等于或小于7,所以小全对小虎的疑问进行了反驳的理由是:碱溶液无论如何稀释,其pH值都不可能小于7;
【方案三】盐酸和锌反应会生成氢气,所以向另一份中先加入过量的NaOH溶液,再加入锌粒中,观察到无气泡产生现象,说明NaOH溶液和HCl溶液发生了反应;
【方案四】在试管中放入NaOH固体,然后加入稀盐酸,小明用手摸了摸试管外壁,试管比较热,他认为不仅说明它们发生了反应,而且是放热反应,小全思考之后仍然不同意小明的观点,理由是:氢氧化钠固体溶于水也放热,乙同学和丙同学各设计了一个装置,都说在不使用温度计的情况下可以判断NaOH溶液与稀盐酸发生了中和反应.分析说明:B装置更合理,理由是:能排除因液体的滴入而造成烧瓶内气体排出,引起玻璃管内液面发生变化,选用合理的装置进行实验,当出现玻璃管中左侧液面下降,右侧液面上升现象时,可以说明NaOH溶液与稀盐酸发生了反应.
故答案为:【方案一】:酚酞(或氢氧化钠溶液),不变红(或变红);
【方案二】:碱溶液无论如何稀释,其pH值都不可能小于7;
【方案三】:无气泡产生;
【方案四】:氢氧化钠固体溶于水也放热;B;能排除因液体的滴入而造成烧瓶内气体排出,引起玻璃管内液面发生变化;玻璃管中左侧液面下降,右侧液面上升.
点评 本题主要考查了化学方程式的书写、酸碱指示剂与溶液相互作用的显色情况及其测定溶液PH方法等方面的知识.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
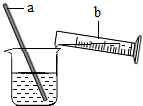 如图是稀释浓硫酸实验的示意图.
如图是稀释浓硫酸实验的示意图.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
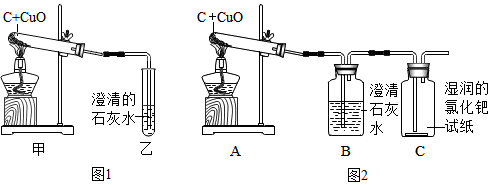
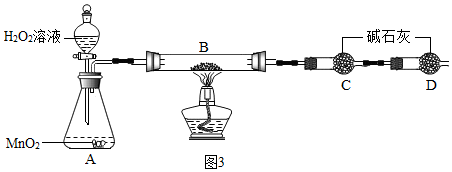
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
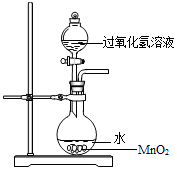 用过氧化氢制氧气时,有同学对事先在烧瓶中加水产生了疑问.他提出了猜想:
用过氧化氢制氧气时,有同学对事先在烧瓶中加水产生了疑问.他提出了猜想:| 实验 | 1 | 2 | 3 | 4 | 5 |
| 过氧化氢溶液溶质质量分数 | 1% | 3% | 5% | 10% | 15% |
| MnO2粉末用量/克 | 0.5 | 0.5 | 0.5 | 0.5 | 0.5 |
| 收集到500mL气体时所用时间/秒 | 560 | 186 | 103 | 35 | 12 |
| 反应后液体温度/℃ | 26 | 38 | 43 | 59 | 71 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
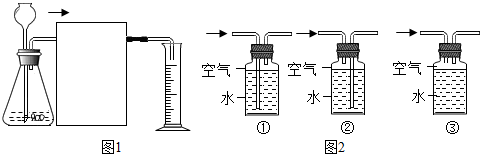
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| A | B | C | D | E | |
| 所放废电池型号 | 1号 | 2号 | 5号 | 7号 | 对照 |
| 金鱼成活时间(天) | 1 | 7 | 15 | 18 | 至今 |
| A | B | C | D | E | |
| 所放废电池型号 | 1号 | 1号 | 1号 | 1号 | 1号 |
| 满江红数量(g) | 0 | 40 | 80 | 120 | 160 |
| 溶解氧(mg/L) | 2.25 | 2.94 | 3.65 | 4.12 | 5.06 |
| 铅(mg/L) | 0.135 | 0.134 | 0.106 | 0.084 | 0.029 |
| 金鱼成活时间(天) | 1 | 8 | 13 | 17 | 至今 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 某学习小组探究氢氧化钙溶液的化学性质,并做了延伸探究.
某学习小组探究氢氧化钙溶液的化学性质,并做了延伸探究.| 方案 | (1) | (2) | (3) |
| 实验操作 | 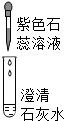 | 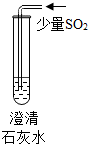 |  |
| 现象 | 溶液变为蓝色 | 澄清石灰水变浑浊 | 红色褪为无色 |
| 结论或解释 | 氢氧化钙溶液能使石蕊等酸碱指示剂变色 | 氢氧化钙溶液能与某些非金属氧化物反应生成盐和水.二氧化硫与澄清石灰水反应的化学方程式是 SO2+Ca(OH)2═CaSO3↓+H2O | 氢氧化钙溶液能与酸发生中和反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验操作 | 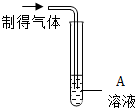 | 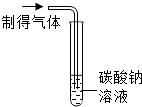 |
| 实验现象 | 出现白色沉淀 | ? |
| 实验结论 | 制得的气体中有氯化氢气体 | 制得的气体中有氯化氢气体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com