
| 温度(℃) | 0 | 20 | 40 | 60 | 80 | 100 |
| NaOH的溶解度(g/100g水) | 42 | 109 | 129 | 174 | 314 | 347 |
| Ca(OH)2的溶解度(g/100g水) | 0.18 | 0.16 | 0.14 | 0.12 | 0.09 | 0.07 |
| 实验步骤 | 实验现象 | 实验结论 |
| 甲同学:用一支洁净的试管取少量固体A,再加入过量稀盐酸. | 有气泡产生 | 自己的猜想 正确 |
| 乙同学:用一支洁净的试管取少量固体A,加水,充分振荡,向上层清液中滴加无色酚酞试液. | 上层清液由无色变为红色 | 自己的猜想 正确 |
分析 【猜想与假设】
氧化钙和水反应能生成氢氧化钙;
【实验与探究】
碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,氢氧化钙和稀盐酸反应生成氯化钙和水;
显碱性的溶液能使酚酞试液变红色;
【反思与评价】
根据实验现象可以判断固体的组成情况;
【表达与交流】
因为固体中含有氢氧化钙,所以B溶液是氢氧化钙的饱和溶液;
氢氧化钙的溶解度随着温度的升高而减小,因此加热氢氧化钙的饱和溶液时,会析出氢氧化钙;
解答 解:(1)[猜想与假设]
氧化钙与水反应生成氢氧化钙,因为氢氧化钙微溶于水,如果氢氧化钙过量时,可能有部分氢氧化钙和碳酸钙一起析出,所以固体A中可能只有碳酸钙,也可能是氢氧化钙和碳酸钙的混合,所以方程式是CaO+H2O═Ca(OH)2;
[实验与探究]
乙同学认为固体A中含有氢氧化钙,那么加入的试剂应该是无色酚酞溶液,酚酞试液变为红色,说明溶液显碱性,含有氢氧化钙.故填:无色酚酞溶液;
[反思与评价]
甲同学的实验不能证明固体A的成分,理由是加入稀盐酸有气泡产生只能证明有CaCO3,不能证明有无Ca(OH)2.故填:加入稀盐酸有气泡产生只能证明有CaCO3,不能证明有无Ca(OH)2.
(2)[表达与交流]
①溶于水的生成物NaOH一定有,而固体中有Ca(OH)2,说明溶液为Ca(OH)2的饱和溶液[或Ca(OH)2微溶于水],所以一定有Ca(OH)2或固体中有Ca(OH)2 即Ca(OH)2过量,所以不会有Na2CO3;
②加热时溶液出现浑浊,是因为B溶液为Ca(OH)2的饱和溶液,Ca(OH)2的溶解度随温度的升高而降低,加热时会析出Ca(OH)2.故填:B溶液为Ca(OH)2的饱和溶液,Ca(OH)2的溶解度随温度的升高而降低,加热时会析出Ca(OH)2.
故答案为:
(1)[猜想与假设]氧化钙与水反应生成氢氧化钙;
[实验与探究]无色酚酞试液;
【反思与评价】不能;加入稀盐酸有气泡只能证明有CaCO3,不能证明有无Ca(OH)2
(2)①因为固体中有Ca(OH)2,说明溶液为Ca(OH)2的饱和溶液;(合理得分)
②B溶液为Ca(OH)2的饱和溶液,加热,Ca(OH)2的溶解度随温度的升高而降低,故析出Ca(OH)2使溶液变浑浊.
点评 化学实验现象是化学实验最突出、最鲜明的部分,也是进行分析推理得出结论的依据,掌握物质的性质和相互之间的反应关系,有助于提高观察实验、进行实验的能力.所以,对化学实验不仅要认真观察,还应掌握设计实验、观察实验现象的方法.


 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案科目:初中化学 来源: 题型:实验探究题

| 实验操作 | 实验现象 | 实验结论 |
| ①按上图组装仪器,装入药品. ②加热铜锈,直至不再有气体产生,停止加热. | 绿色固体变为黑色;硫酸铜粉末变为蓝色;烧杯中液体变浑浊. | 加热铜锈生成的物质有氧化铜、水和二氧化碳;铜锈由铜、碳、氢、氧元素组成;烧杯中发生反应的化学方程式为CO2+Ca(OH)2═CaCO3↓+H2O. |
| ③冷却后,向试管中固体加入适量稀硫酸,稍加热. | 黑色固体溶解,溶液变为蓝色. |
| 序号 | 实验内容 | 实验结论 | 实验反思 |
| 实验1 | 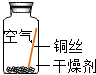 | 在干燥环境中,铜不易生锈. | (1)实验2和3中使用的是经煮沸后迅速冷却的蒸馏水,其原因是除去水中溶解的氧气. (2)如果要证明铜生锈的快慢是否与二氧化碳的浓度有关,还需要补充的一个实验内容是在含量高的二氧化碳的空气中,将铜丝放入蒸馏水中. |
| 实验2 | 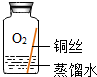 | 在没有二氧化碳的情况下,铜不易生锈. | |
| 实验3 | 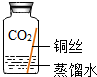 | 在没有氧气的情况下,铜不易生锈. | |
| 实验4 | 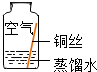 | 铜生锈的条件是铜与水、氧气、二氧化碳等物质充分接触. |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
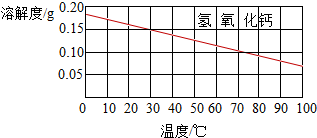
| A. | 所得溶液质量为100.5g | B. | 所得溶液是不饱和溶液 | ||
| C. | 降低温度溶液的质量变大 | D. | 升高温度溶液溶质质量分数变大 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | CH4、CH3COOH、C6H12O6都属于有机化合物 | |
| B. | 棉花、羊毛、塑料都属于天然有机高分子材料 | |
| C. | 熟石灰、烧碱、浓硫酸都可以用作干燥剂 | |
| D. | CO(NH2)2、KNO3,Ca(H2PO4)2都属于复合肥料 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 溶液都是无色透明的液体 | |
| B. | 固体NaOH溶于水时,溶液温度升高 | |
| C. | 饱和溶液的质量分数一定比不饱和溶液的质量分数大 | |
| D. | 60℃时硝酸钾的溶解度为110g,其溶液中溶质与溶剂的质量比为11:21 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 利用金属锰和FeCl2溶液进行实验 | |
| B. | 利用大小相同的锰片和铁片分别与稀硫酸反应 | |
| C. | 利用金属铁和MnSO4溶液进行实验 | |
| D. | 查阅初中化学课本上的金属活动顺序表 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 因为碱溶液呈碱性,所以呈碱性的溶液一定都是碱溶液 | |
| B. | 因为蜡烛燃烧生成CO2和H2O,所以蜡烛组成里一定含有碳元素和氢元素 | |
| C. | 因为燃烧需要同时满足三个条件,所以灭火也要同时破坏这三个条件 | |
| D. | 因为中和反应生成盐和水,所以有盐和水的反应一定是中和反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com