
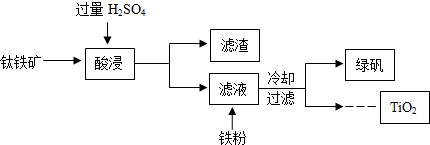
分析 (1)由Fe2O3与稀硫酸反应生成硫酸铁和水,进行分析解答.
(2)加入铁粉,铁粉能与过量的稀硫酸生成硫酸亚铁溶液和氢气,写出反应的化学方程式即可.
(3)由质量守恒定律:反应前后,原子种类、数目均不变,进行分析解答.
解答 解:(1)Fe2O3与稀硫酸反应生成硫酸铁和水,反应的化学方程式是:Fe2O3+3H2SO4═Fe2(SO4)3+3H2O.
(2)加入铁粉,铁粉能与过量的稀硫酸生成硫酸亚铁溶液和氢气,反应的化学方程式为:Fe+H2SO4═FeSO4+H2↑.
(3)由质量守恒定律:反应前后,原子种类、数目均不变,由反应的化学方程式,反应前钛、氧、氯、碳原子个数分别为1、2、4、1,反应后的生成物中钛、氧、氯、碳原子个数分别为1、0、4、1、根据反应前后原子种类、数目不变,则每个横线上物质的分子由2个氢原子和1个氧原子构成,则物质X的化学式为CO2.
故答案为:(1)Fe2O3+3H2SO4═Fe2(SO4)3+3H2O;(2)Fe+H2SO4═FeSO4+H2↑;(3)CO2.
点评 本题难度不大,理解用钛铁矿作原料制取二氧化钛及绿矾的反应流程,掌握酸与金属的化学性质、化学方程式的书写方法等是正确解答本题的关键.


 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案科目:初中化学 来源: 题型:选择题
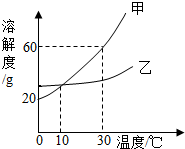 如图是甲、乙两种固体的溶解度曲线,下列说法正确的是( )
如图是甲、乙两种固体的溶解度曲线,下列说法正确的是( )| A. | 甲的溶解度大于乙的溶解度 | |
| B. | 10℃时,等质量的甲乙溶液中溶质质量分数相等 | |
| C. | 20℃时,将10g甲物质加入50g水中,得到60g溶液 | |
| D. | 30℃时,配制质量分数为60%的甲溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
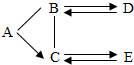 已知A、B、C、D、E是初中化学常见的不同类别的物质.C的水溶液呈蓝色,D是一种红色固体,B→D的反应过程较为复杂,D→B的反应用于冶金工业.中“-”表示相连物质可以发生反应,“→”表示一种物质生成另一种物质(部分反应物、生成物及反应条件省略).
已知A、B、C、D、E是初中化学常见的不同类别的物质.C的水溶液呈蓝色,D是一种红色固体,B→D的反应过程较为复杂,D→B的反应用于冶金工业.中“-”表示相连物质可以发生反应,“→”表示一种物质生成另一种物质(部分反应物、生成物及反应条件省略).查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 海水晒盐 | B. | 木头制作家具 | C. | 水力发电 | D. | 冶炼铜矿 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 实验内容 | 操作或所用试剂 |
| A | 鉴别铁粉和木炭粉 | 观察颜色 |
| B | 除去氯化钾溶液中的硫酸钾 | 加入适量氯化钡溶液,过滤 |
| C | 鉴别羊毛和合成纤维 | 取样、灼烧,闻气味 |
| D | 鉴别氮气和氧气 | 燃着的木条 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 物质 | NH3 | NO | NO2 | SO2 | SO3 |
| 一些特性 | 碱性 | 在空气中会迅速变成 NO2 | 红棕色 | 酸性,有刺激性气味,能使 KMnO4溶液褪色 | 沸点 44.8℃ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com