
| A�� | ��ɫ��ĩ��һ�������Ȼ��� | |
| B�� | ��ɫ��ҺB��ֻ����һ������ | |
| C�� | ��������ɵ���������������4.4g | |
| D�� | ��ɫ��ĩ�в���̼��ơ������ơ�����ͭ |
���� ����̼���������ˮ������ͭ����Һ������ɫ����������Ӻͱ����ӻ��������ᱵ���������ᱵ�����������ᣬ̼������Ӻͱ����ӻ�����̼�ᱵ������̼�ᱵ���������ᣬ�����Ӻ������ӻ����ɲ���������Ȼ���������֪ʶ���з�����
��� �⣺��ȡһ�������ĸð�ɫ��ĩ������ˮ�ܽ⣬����ɫ��ҺA��̼���������ˮ������ͭ����Һ������ɫ������ɫ��ĩ��һ������̼��ơ�����ͭ������ɫ��ҺA�м�������Ȼ�����Һ����ַ�Ӧ����ˣ��ֱ����ɫ��ҺB�Ͱ�ɫ����C������ɫ����Cϴ�ӣ���ɺ�Ƶ�����Ϊ20g����20g��ɫ����C�м���������ϡ���ᣬ����������ʧ����������ð����˵����ɫ����C�����ᱵ������̼�ᱵ�����Ļ�������ɫ��ĩ��һ������̼���ơ������ƣ�̼���ƺ��Ȼ�������̼�ᱵ�������Ȼ��ƣ������ƺ��Ȼ����������ᱵ�������Ȼ��ƣ��Ȼ����ǹ����ģ�����B�е��������Ȼ��ƺ��Ȼ���������ɫ��ҺB�еμ���������Һ��ϡ���ᣬ������ɫ������˵����ҺB�к��������ӣ����Ǽ�����Ȼ��������������ӣ���ɫ��ĩ���Ƿ����Ȼ��ƣ�����Ӱ��ʵ����������ɫ��ĩ�п��ܺ����Ȼ��ƣ�
A��ͨ���Ƶ���֪����ɫ��ĩ�п��ܺ����Ȼ��ƣ���A����
B��ͨ���Ƶ���֪����ɫ��ҺB���������Ȼ��ƺ��Ȼ���������ֻ����һ�����ʣ���B����
C��ͨ������ʽ��BaCO3+2HCl=BaCl2+H2O+CO2�������Կ���������4.4�˵Ķ�����̼����Ҫ̼�ᱵ19.7�ˣ�������Ϊ20g����C��ȷ��
D��ͨ���Ƶ���֪����ɫ��ĩ�в���̼��ơ�����ͭ����D����
��ѡ��C��
���� �ڽ������ʱ�����ȷ��������������ʵ����ʺ�����֮��ķ�Ӧ��Ȼ���������е������жϸ����ʵĴ����ԣ���������֤���ɣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ���� | ��ѡ�Լ����������� |
| A | Cu��CuO�� | ͨ������������ |
| B | CO2��HCl�� | ����ͨ��ʢ����������������Һ��ϴ��ƿ |
| C | N2��O2�� | ����ͨ�����ȵ�ͭ�� |
| D | KCl��Һ��K2CO3�� | ��������Ȼ�����Һ��ַ�Ӧ����� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
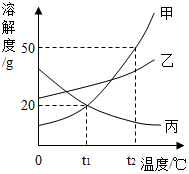 ��ͼ�Ǽס��ҡ������ֹ������ʵ��ܽ�����ߣ�����˵��������ǣ�������
��ͼ�Ǽס��ҡ������ֹ������ʵ��ܽ�����ߣ�����˵��������ǣ�������| A�� | t1��ʱ���ס����������ʵı�����Һ��������������ͬ | |
| B�� | Ҫ�Ӽ����ʵı�����Һ�л�þ���ף����Բ��ý��µķ��� | |
| C�� | t2��ʱ��30g���뵽50gˮ�г���ܽ⣬������Һ��������������Ϊ37.5% | |
| D�� | ���������ʵı�����Һ��t2�潵����t1�棬������Һ���������������ң��ף��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Fe2O3��FeCl2 | B�� | CaCO3��CaCl2 | C�� | H2O2��H2O | D�� | CO2��O2 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com