19、粗食盐中除含有钙、镁、硫酸根等可溶性杂质外,还含有泥砂等不溶性杂质.
实验室中粗食盐提纯的操作如下:
(1)在台称上称取租食盐15克,研细,放入小烧杯中,加40毫升蒸馏水,用电炉加热并搅拌,使其溶解.然后往热溶液中加入3~4毫升25%的BaCl
2溶液.小心用电炉保温10分钟,使BaSO
4沉淀完全.请问:如何运用最简方法检验溶液中已无SO
42-离子?
静止片刻在上层清液处,滴加一滴BaCl2溶液,不出现浑浊就说明SO42-已经除尽
;
(2)在上述溶液中滴加饱和Na
2CO
3溶液,直至不再产生沉淀为止.请问这步操作的目的是
除去Ca2+、Mg2+以及加入过量Ba2+
;
(3)将经过操作(2)后的溶液趁热进行减压过滤.请问这一操作能除掉哪些杂质?
BaSO4、CaCO3、MgCO3、BaCO3以及泥砂等不溶性杂质
;
(4)用纯净氯化氢通入操作(3)所得滤液中,直至不再析出NaCl晶体为止.通氯化氢气体的作用是
除去溶液中的CO32-,同离子效应使NaCl结晶析出
;
(5)用减压过滤方法将产品(NaCl晶体)抽干,并将产品移入蒸发皿,在通风橱中炒干.请问烘炒的原因是
去掉吸附在晶体表面的HCl
.

 =
=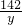 =
=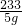 =
=
 ×100%=5%
×100%=5%

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案