
| 中和试剂 | 氢氧化钠 | 氢氧化钙 |
| 价格/(元•吨-1) | 800 | 450 |
分析 (1)根据所给的途中信息可以知道,等量的氢氧化钙价钱更低,氢氧化钙和硫酸反应生成了微溶于水的硫酸钙,在水中的残留更少,可以据此解答该题;
(2)氨水和硫酸反应能够生成硫酸铵,但是硫酸铵会溶于水,而难以全部回收,从而使水体富营养化,可以据此解答.
解答 解:(1)H2SO4+2NaOH═Na2SO4+2H2O H2SO4+Ca(OH)2═CaSO4+2H2O
98 80 98 74
根据上述化学方程式可以判断,消耗等质量的硫酸需要的氢氧化钙的质量更少,同时反应生成了微溶于水的硫酸钙,结合表格中可以知道等量的氢氧化钙价钱更低,氢氧化钙和硫酸反应生成了微溶于水的硫酸钙,在水中的残留更少;
(2)氨水和硫酸反应能够生成硫酸铵,但是硫酸铵会溶于水,而难以全部回收,从而使水体富营养化,分析所给的选项可以知道选项C是正确的,故选C.
故答案为:(1)①中和等量硫酸时所用Ca(OH)2更少,费用更低;②用Ca(OH)2中和H2SO4产物为微溶的CaSO4,在水体中残留较少.(2)C.
点评 本题较好考查了学生实验设计和依据题目所给信息,分析、解决问题的能力,通过解答本题体会到设计实验时要尽量做到严谨,可以通过对比实验解决问题.


科目:初中化学 来源: 题型:选择题
| A. | AgS | B. | Ag2S | C. | Ag2O2 | D. | Ag2O |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 1:2 | B. | 1:1 | C. | 32:1 | D. | 4:1 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
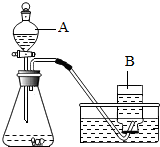 在实验室里,常用分解过氧化氢溶液制取氧气,某兴趣小组对氧气的实验室制取法进行了探究.
在实验室里,常用分解过氧化氢溶液制取氧气,某兴趣小组对氧气的实验室制取法进行了探究.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 一氧化碳可以冶炼金属,是由于一氧化碳具有可燃性 | |
| B. | 工业上常用稀硫酸除去铁锈,是由于稀硫酸能与铁反应 | |
| C. | 洗涤剂常用来洗涤油污,是因为洗涤剂有乳化功能 | |
| D. | 稀有气体中的氦可用于填充气球,是由于氦的化学性质不活泼 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 缺铁会患贫血症 | B. | 纤维素不属于糖类 | ||
| C. | 摄入淀粉量不足,会患低血糖 | D. | 食用蔬菜、水果可以补充维生素 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
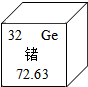 锗是重要的半导体材料,锗元素的相关信息如图,下列有关锗的说法正确的是( )
锗是重要的半导体材料,锗元素的相关信息如图,下列有关锗的说法正确的是( )| A. | 属于非金属元素 | B. | 核电荷数为32 | ||
| C. | 原子序数为40 | D. | 相对原子质量为72.63g |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 同学们发现将NaOH溶液和稀盐酸混合后没有明显现象,为了证明NaOH能与HCl发生中和反应,设计了如下实验:
同学们发现将NaOH溶液和稀盐酸混合后没有明显现象,为了证明NaOH能与HCl发生中和反应,设计了如下实验:| 实验步骤 | 现象 | 结论 |
| 实验1.取少量NaOH溶液于试管中,向其中滴加几滴无色酚酞试液,振荡. | 溶液呈红色 | |
| 实验2.向实验1的试管中加入适量的稀盐酸,振荡. | 红色逐渐消失. | NaOH与HCl能反应. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com