
生产和生活中的下列物质,属于纯净物的是
A. 浓硫酸 B. 冰水 C. 无烟煤 D. 铝合金
B 【解析】A、浓硫酸是由硫酸和水组成的,属于混合物;B、冰是固态的水,冰水属于同一种物质,冰水属于纯净物;C、无烟煤主要含有碳,还含有少量的硫、磷、氢、氮、氧等,是由有机物和无机物所组成的复杂混合物;D、铝合金中有铝和其它成分,属于混合物。故选B。科目:初中化学 来源:福建省2018届质检化学试卷 题型:单选题
下图是水在电解过程中发生变化的微观示意图,下列说法正确的是
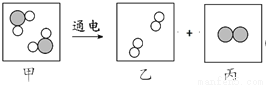
A. 与负极相连玻璃管内产生的物质是乙
B. 实验说明水是由氢气和氧气组成
C. 反应前后分子、原子种类及数目均不变
D. 甲、乙、丙三种物质的质量比是2∶2∶1
A 【解析】电解水时,正氧负氢,氢二氧一。根据反应的微观示意图,该反应中,乙是氢气,丙是氧气。A. 与负极相连玻璃管内产生的物质是氢气,正确;B. 实验说明水由氢元素和氧元素组成,错误;C. 反应前后原子种类及数目均不变,分子种类及数目发生改变,错误;D. 甲、乙、丙三种物质的质量比是9∶1∶8,错误。故选A。查看答案和解析>>
科目:初中化学 来源:辽宁省大连市毕业升学模拟化学试卷 题型:单选题
下图是铊元素在元素周期表中的相关信息,下列说法错误的是

A. 铊原子中的质子数是81 B. 铊属于金属元素
C. 铊的原子序数是81 D. 铊的原子质量是204.4
D 【解析】A、由元素周期表的信息可知,铊元素的原子序数为81,因为原子序数=核电荷数=质子数,故质子数为81,故正确;B、由铊的元素名称的汉字偏旁为“金”,则属于金属元素,故正确;C、由元素周期表的信息可知,铊元素的原子序数为81,故正确;D、由元素周期表的信息可知,铊的相对原子质量是204.4,故错误。故选D。查看答案和解析>>
科目:初中化学 来源:湖北省鄂州市梁子湖区2018届九年级下学期期中考试理综化学试卷 题型:简答题
生活处处有化学。请用所学化学知识填空:
(1)家庭生活中欲降低水的硬度常用__________;
(2)洗洁精能洗去餐桌上的油污是由于洗洁精具有__________功能;
(3)成语“釜底抽薪”应用的灭火原理是__________;
(4)铝制品具有优良的抗腐蚀性,原因是__________。
煮沸 乳化 撤离可燃物 铝能和空气中的氧气反应生成致密的氧化铝保护膜,阻止铝继续与氧气反应 【解析】本题考查了水净化方法,乳化的应用,灭火的原理,铝的化学性质。 (1) 加热煮沸能使可溶性钙镁化合物转化为不溶性钙镁化合物,降低了水的硬度。家庭生活中欲降低水的硬度常用煮沸; (2) 洗洁精具有乳化功能,把油污分解为小液滴。洗洁精能洗去餐桌上的油污是由于洗洁精具有乳化功能; (...查看答案和解析>>
科目:初中化学 来源:湖北省鄂州市梁子湖区2018届九年级下学期期中考试理综化学试卷 题型:单选题
在只含有NH4+、Na+、Cl-、SO42-的溶液中能存在的离子是
A. OH- B. Ba2+ C. Ag+ D. NO3-
D 【解析】A、OH-与溶液中的NH4+结合放出氨气,OH-不能在此溶液中存在,错误;B、Ba2+与溶液中的SO42-结合生成硫酸钡的沉淀,Ba2+不能在此溶液中存在,错误;C、Ag+与溶液中的Cl-结合生成氯化银沉淀,Ag+不能在此溶液中存在,错误;D、NO3-与溶液中的离子不能形成沉淀、气体、水,NO3-能在此溶液中存在,正确。故选D。查看答案和解析>>
科目:初中化学 来源:广东省汕头市毕业生学业考试模拟化学试卷 题型:科学探究题
某实验小组的甲、乙两同学围绕Na2CO3进行了如图一所示的实验.实验结束后,丙同学把A、B两支试管中的物质倒入同一洁净的烧杯中(如图二),充分混合后发现白色沉淀明显增加,结合题目信息,回答以下问题:

(1)甲同学的实验完成后,A试管一定有剩余的物质是_________。
(2)B试管的实验发生的化学方程式是________________。
小组同学将C中液体过滤后,对所得滤液的主要成分进行了如下探究:
【猜想与假设】实验小组的同学对滤液的成分作出了如下猜想:
猜想一:滤液中的溶质是NaCl、Na2CO3
猜想二:滤液中的溶质是_______。。
猜想三:滤液中的溶质是NaCl、CaCl2、Na2CO3
猜想四:滤液中的溶质是NaCl
【讨论与交流】通过认真讨论,小组同学排除了其中一种不合理的猜想。
(3)你认为不合理的猜想是_______,理由是______。
【进行实验】丁同学取少量滤液置于试管中,向试管中滴加一种物质,发现有无色气泡生成。
(4)你认为丁同学向滤液中滴加的物质是_________。
【实验结论】通过探究,小组同学得出了猜想一成立的结论。
碳酸钠 Na2CO3+CaCl2=CaCO3↓+2NaCl NaCl、CaCl2 猜想三 CaCl2、Na2CO3不能在溶液中共存 稀盐酸或稀硫酸 【解析】甲中稀盐酸和碳酸钠反应生成氯化钠、水和二氧化碳,乙中碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠,丙同学把A、B两支试管中的物质倒入同一洁净的烧杯中(如图二),充分混合后发现白色沉淀明显增加,说明甲中碳酸钠过量,乙中氯化钙过量;碳酸钠能和稀盐...查看答案和解析>>
科目:初中化学 来源:广东省汕头市毕业生学业考试模拟化学试卷 题型:填空题
二氧化硫是大气的主要污染物,严禁直接排放,工业上常用 NaOH溶液来吸收。
(1)写出NaOH溶液吸收SO2的化学方程式________。
(2)图中小球分别表示NaOH溶液及吸收SO2后所得溶液中溶质的微粒,其中“ ”表示的微粒是________。
”表示的微粒是________。

查看答案和解析>>
科目:初中化学 来源:上海市宝山&嘉定区2018年初三化学二模试卷 题型:实验题
利用下列提供的仪器装置回答问题:
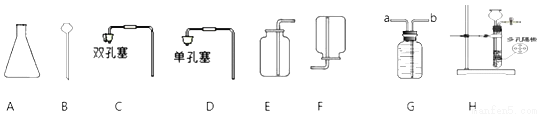
①仪器名称:A为_____
②小丽用双氧水和二氧化锰制取氧气时,发现反应速率过快,小丽思考后将所用仪器B改为_____,该反应的化学方程式为_____,若使用装置G收集氧气,氧气应从_____(填“a”或“b”)端通入。
③小明选用A到G中仪器,组装出实验室制取二氧化碳装置,他所选仪器有_____(填写一套即可),反应的化学方程式为_____。
④小刚选用H装置放入锌粒和稀硫酸制取氢气,H装置的优点是_____,反应一段时间后他关闭活塞,发现装置中固液无法分离,原因可能为_____(写出一种即可);
⑤小刚用制得的氢气还原氧化铜,得到0.1mol铜,则理论上参与反应的氢气的质量为_____(根据化学方程式计算)。
锥形瓶 分液漏斗 2H2O22H2O+O2↑ a ABCE CaCO3+2HCl═CaCl2+H2O+CO2↑ 能控制反应的发生和停止 硫酸反应完了 0.2g 【解析】①仪器A的名称为锥形瓶; ②仪器B是分液漏斗,该仪器不能控制反应的速率,将长颈漏斗改为分液漏斗可以控制加入过氧化氢的速率,从而可以控制反应的速率;该反应是过氧化氢在二氧化锰作催化剂的条件下反应生成氧气和水,反应方程式为2...查看答案和解析>>
科目:初中化学 来源:江苏省苏州市2018届九年级第二次模拟测试化学试卷(2) 题型:单选题
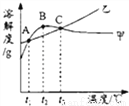
NH4Cl和Na2SO4的溶解度表及溶解度曲线如图.下列说法错误的是( )
温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | |
溶解度S/g | NH4Cl | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 60.2 |
Na2SO4 | 9.6 | 20.2 | 40.8 | 48.4 | 47.5 | 47.0 |
A. 乙为NH4Cl
B. t3应介于40℃﹣50℃
C. 55℃时,分别将两饱和溶液蒸发等质量的水,得到固体质量甲>乙
D. 等质量的甲、乙饱和溶液从t3降温到t1,析出的晶体质量相等
C 【解析】A、通过分析表中的数据可知,氯化铵的溶解度随温度的升高逐渐增大,所以乙为氯化铵,正确;B、通过分析表中的数据可知,甲的溶解度在t2℃时,溶解度达到最大,在t3℃时,甲、乙的溶解度相等,所以t3℃应介于40℃-50℃,正确;C、55℃时,甲的溶解度小于乙的溶解度,所以分别将两饱和溶液蒸发等质量的水,得到固体质量甲<乙,错误; D、t3℃、t1℃甲、乙的溶解度相等,所以等质量的...查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com