
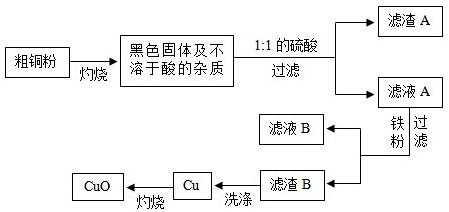
分析 (1)配制1:1的硫酸溶液所需的玻璃仪器除玻璃棒外,还需要烧杯、量筒,利用量筒可以量取一定量的液体.
(2)氧化铜和稀硫酸反应生成硫酸铜和水;
(3)滤渣B中含有铜和过量的铁粉,铁能和稀硫酸反应生成硫酸亚铁和氢气;
(4)知道氧化铜的质量,可以计算铜元素的质量,铜元素质量和粗铜粉质量的比值即为粗铜粉中Cu的含量.
解答 解:(1)1:1的H2SO4是用1体积98%的H2SO4与1体积水混合而成.配制该硫酸溶液所需的玻璃仪器除玻璃棒外,还需要烧杯、量筒.
故填:量筒.
(2)黑色固体是氧化铜,和稀硫酸反应的化学方程式为:CuO+H2SO4═CuSO4+H2O.
故填:CuO+H2SO4═CuSO4+H2O.
(3)在洗涤操作中,可以用稀硫酸洗涤滤渣B,滤渣知道铁能和稀硫酸反应,铜不能和稀硫酸反应.
故填:H2SO4.
(4)若不考虑生产过程中的损耗,要计算粗铜粉中Cu的含量,需要测定的数据是:最终所得氧化铜的质量和粗铜粉的质量.
故填:粗铜粉的质量.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.


 通城学典默写能手系列答案
通城学典默写能手系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 实验室中氯化钡废液可直接排入下水道 | |
| B. | 利用2Cu+O2+2H2SO4(稀)═2CuSO4+2H2O的反应由铜制取胆矾 | |
| C. | 在煤矿附近建发电厂有利于减少二氧化硫排放 | |
| D. | 用废旧塑料制食品包装袋以减少“白色污染” |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

| 物 质 | Cu(OH)2 | Fe (OH)3 |
| 开始沉淀pH | 4.2 | 1.2 |
| 完全沉淀pH | 6.7 | 3.2 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 10 ml的量筒 | B. | 100 ml的量筒 | ||
| C. | 50 ml的量筒和胶头滴管 | D. | 500 ml的量筒和胶头滴管 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com