
【题目】现有锌、氦气、氯化钠、甲烷、氧化钙五种物质,请按要求填空:
(1)氮气可用于制造低温环境,它的化学式是___________。
(2)氯化钠可用于配制生理盐水,其溶液中的阴离子是___________(填离子符号)。
(3)氧化钙可用作食品干燥剂,其原理是___________(填“物理”或“化学”)变化。
(4)甲烷可用作燃料,其反应原理是______________________(填化学方程式)。
(5)锌常用于实验室中与盐酸反应制取氢气,其反应原理是________(填化学方程式)。
【答案】N2 Cl- 化学 CH4 + 2O2 ![]() CO2 + 2H2O Zn+2HCl==ZnCl2+H2↑
CO2 + 2H2O Zn+2HCl==ZnCl2+H2↑
【解析】
(1) 单质的化学式的书写:在元素符号右下角标上一个分子中原子的个数,氮气可用于制造低温环境,它的化学式是N2;
(2) 离子符号书写:元素(或根)符号右上角的数字表示一个离子带电荷的数值,数字在左,正负号在右,电荷数为1时,1不写;氯化钠可用于配制生理盐水,其溶液中的阴离子是氯离子,符号为Cl-;
(3)氧化钙可用作食品干燥剂,其原理是氧化钙和水反应,放出大量热,因由新的物质生成是化学变化;
(4)甲烷可用作燃料,其反应原理是CH4 + 2O2 ![]() CO2 + 2H2O;
CO2 + 2H2O;
(5)锌常用于实验室中与盐酸反应制取氢气,其反应原理是锌和盐酸反应生成氢气和氯化锌,化学方程:Zn+2HCl==ZnCl2+H2↑。


 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:初中化学 来源: 题型:
【题目】纳米级超细碳酸钙是一种新型超细固体材料,是橡胶、塑料制品、造纸、涂料、油墨等工业重要填料。工业上用石灰石来制备纳米级超细碳酸钙的流程如下图,请回答下列问题:

Ⅰ.煅烧炉中发生反应的化学方程式是 (28) 。操作1、2与实验室 (29) 操作类似。
Ⅱ.沉淀池中反应的基本类型属于 (30) 。石灰乳一般是在氧化钙中加水生成的,存在着还没有溶解的氢氧化钙,则石灰乳是 (31) (填:溶液、悬浊液、乳浊液)。
Ⅲ.上述流程中可循环使用的物质的化学式为 (32) 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业铁红的主要成分是Fe2O3,还含有少量的FeO、Fe3O4。为了测定铁红中铁的质量分数,兴趣小组的同学进行了如下实验,请你参与过程分析。
(资料1)草酸晶体(H2C2O4·3H2O)在浓H2SO4作用下受热分解,化学方程式为H2C2O4·3H2O![]() CO2↑+CO↑+4H2O
CO2↑+CO↑+4H2O
(问题讨论)用下图所示装置进行实验:
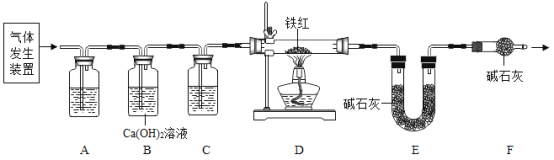
(1)实验前应先检查装置的气密性。
(2)进入D中的气体是纯净、干燥的CO,则A、C中的试剂依次是_____(填字母编号)。
a 浓硫酸 b 澄清的石灰水 c 氢氧化钠溶液
(3)B装置的作用是________。
(4)对D装置加热前和停止加热后,都要通入过量的CO,其作用分别是:
①加热前将装置中的空气排出,防止发生爆炸。
②停止加热后_________。
(5)写出D装置中所发生反应的一个化学方程式____。
(数据分析与计算)
(资料2)铁的常见氧化物中铁的质量分数:
铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
铁的质量分数 | 77.8% | 70.0% | 72.4% |
(6)称取铁红样品10.0g,用上述装置进行实验,测定铁红中铁的质量分数。
①D中充分反应后得到Fe粉的质量为mg。
②实验前后称得E装置增重6.6g,则此铁红中铁的质量分数是_____。
(实验评价)
本实验中如果缺少C装置(不考虑其它因素),则测得样品中铁的质量分数会____(填“偏小”、“不变”或“偏大”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】以下是有关气体制取以及性质实验的装置,试回答下列问题:
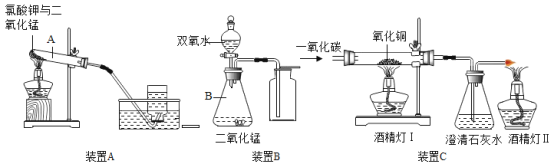
①写出编号仪器的名称:A.___,B___。
②用装置A.制取氧气,写出发生反应的化学方程式__,判断氧气已收集满的方法是__。反应结束时,若未将导管从水中移走就熄灭了酒精灯,可能的后果是___。
③若用B作制取氧气的发生装置,分液漏斗的作用是____。(填入相应字母)
A 便于添加试剂。
B 通过控制滴加试剂的速率,控制双氧水的反应速率。
C 通过控制滴加试剂的速率,使反应能保持较平稳地进行。
④ 写出装置C中一氧化碳和氧化铜反应的化学方程式____。关于装置C的实验,下列说法正确的是____。
A 酒精灯Ⅱ需要在气体纯净后方可点燃。
B 酒精灯Ⅱ的作用是将反应后气体中的一氧化碳点燃,防止有毒气体的排放。
C 实验结束时应先熄灭酒精灯,待冷却到室温后再停止通入一氧化碳。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】测定某品牌洁厕灵中硫酸质量。取20g该品牌的洁厕灵溶液于烧杯中,不断滴加25g溶质质量分数为17.1%的氢氧化钡溶液,反应过程中滴入氢氧化钡溶液的质量和烧杯中溶液pH变化的部分数据如下所示:
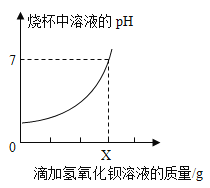
滴加氢氧化钡溶液的质量/g | 5 | 10 | X | 25 |
烧杯中产生沉淀的质量/g | 1.165 | 2.33 | 4.66 | 4.66 |
求:
①当烧杯中溶液的pH=7时,加入氢氧化钡溶液质量X=______g。
②测得20g该品牌的洁厕灵溶液中硫酸的质量是______g。(根据化学方程式计算)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图表示某些物质间转化关系(反应条件和部分产物已省略)。其中A、E为固体氧化物,且A为黑色粉末,E是红棕色固体;B、D是由相同元素组成的无色液体,且B具有消毒杀菌作用;C、Y、Z为无色气体,其中Y有毒;X是最常见的金属。请回答下列问题:
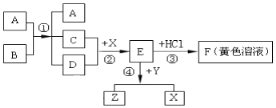
(1)反应①中A物质的作用是__________;
(2)反应③、④的化学方程式: ③________________;④__________________________;
(3)在日常生活中为防止反应②的发生,可采取的措施是______________(写一点即可);
(4)C的用途是_______________________(写一点即可)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在利用红磷燃烧测定空气中氧气含量的实验中用传感器记录集气瓶中压强、温度随时间的变化情况如图所示,其中a是打开止水夹的时刻。下列说法不正确的是( )
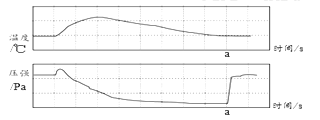
A. a时处的压强等于大气压B. 反应开始压强增大是因为温度升高
C. a时的温度已经接近室温D. a时以后气压增大是由于水倒吸入集气瓶
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】阅读下面科普短文![]() 改编自屠呦呦2015年12月7日瑞典演讲稿
改编自屠呦呦2015年12月7日瑞典演讲稿![]() 。
。
很多中药古方都提到了青蒿入药抗疟疾,但当1971年开始从青蒿中提取有效成分时,结果却总是不理想,屠呦呦研究组反复研究中医古籍,其中“青蒿一握,以水两升渍,绞取汁,尽服之“激发了她的灵感,是不是高温下破坏了青蒿中抗疟的有效成分?屠呦呦立即改用乙醚在较低温度下进行提取,成功获得了抗疟有效单体的提纯物质,命名为青蒿素。
完成样品纯化后,通过元素分析、光谱测定、质谱及旋光分析等技术手段,测定相对分子质量为282,得出了青蒿素的化学式。但青蒿素的具体结构是什么样的呢?有机所得专家做了一个定性实验,加入碘化钾后,青蒿素溶液变黄了,说明青蒿素中含有过氧基团;而后专家又通过X射线衍射法等方法,最终确定了青蒿素是含有过氧基的新型倍半萜内酯。
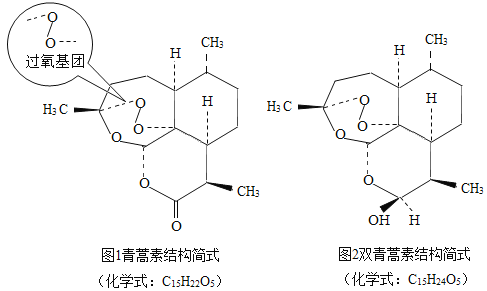
由于自然界中天然青蒿素的资源是有限的,接下来就要把自然界的分子通过人工合成制成药物,在这一过程中,研究组又有一项重大研究成果,获得了青蒿素的衍生物,衍生物之一是双氢青蒿素,它也具有抗疟的疗效,并且更加稳定,水溶性好,比青蒿素的疗效好,10倍,进一步体现了青蒿素类药物“高效、速效、低毒”的特点。
依据文章内容,回答下列问题:
(1)从中国古代青蒿入药,到2004年青蒿素类药物被世界卫生组织列为对抗疟疾的首选药物,经历了漫长的历程。将下列三项针对青蒿素的研究按时间先后排序______(填数字序号)。
①确定结构 ②分离提纯 ③人工合成
(2)屠呦呦用乙醚提取青蒿素,获得成功的关键在于改变了哪种条件:______。
(3)向无色的双氢青蒿素溶液中加入碘化钾,实验现象为______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com