
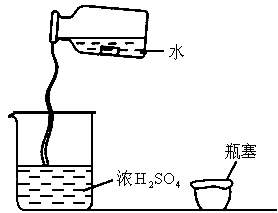
如下图为某同学稀释浓硫酸的实验操作,其中有四处主要错误,请改正过来.
(1)____________________________________
;(2)____________________________________
;(3)____________________________________
;(4)____________________________________
.|
(1) 瓶塞应倒放(2) 试剂瓶上的标签应向着手心(3) 应将浓硫酸倒入水里(4) 应将浓硫酸沿着容器壁慢慢地注入水里,并用玻璃棒不断搅拌解析:液体药品通常盛放在细口瓶里,取用细口瓶里的药液时,先拿下瓶塞,倒放在桌上,并且标签应向着手心,如果瓶塞正放会污染瓶塞,同时也会腐蚀桌面,标签如果不向着手心,残留在瓶口的药液流下会腐蚀标签,用完之后,应把瓶子放回原处,标签向外.浓硫酸溶于水时放出大量的热,因此稀释浓硫酸时应将浓硫酸沿着容器壁慢慢地注入水里,并用玻璃棒不断搅拌,使产生的热量迅速扩散,防止液体暴沸溅出,切不可将水倒进浓硫酸里. |
|
点拨:此题考查了实验基本操作及稀释浓硫酸的方法,做实验必须严格按照实验操作规程,否则会影响实验效果或造成事故. |


科目:初中化学 来源: 题型:阅读理解
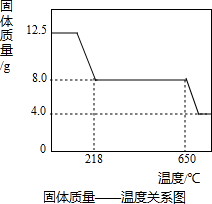 某企业是一家以生产电缆类产品为主的地方明星企业.在电缆生产过程中,不可避免地会产生一定量的含铜废料(如:零碎电缆).某化学兴趣小组的同学得知这一情况后,提出可以用含铜废料制备胆矾(CuSO4?5H2O).
某企业是一家以生产电缆类产品为主的地方明星企业.在电缆生产过程中,不可避免地会产生一定量的含铜废料(如:零碎电缆).某化学兴趣小组的同学得知这一情况后,提出可以用含铜废料制备胆矾(CuSO4?5H2O).

查看答案和解析>>
科目:初中化学 来源:广西柳州市2012届九年级第一次教学质量检测化学试题 题型:038
现有一瓶未开启的浓硫酸,试剂瓶标签上的部分内容如图所示.

(1)H2SO4的相对分子质量是________.
(2)H2SO4分子中,H、S、O的原子个数比为________.
(3)该瓶浓硫酸的质量为________g.
(4)用100 g98%的该浓硫酸稀释成19.6%的稀硫酸,需要水多少g?
(5)某同学用锌粒与19.6%的稀硫酸反应制取氢气,反应所用的稀硫酸和生成氢气的关系如下图.
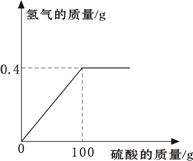
计算:
①至少需要多少g的锌粒?
②完全反应后所得溶液的溶质质量分数为多少?(保留一位小数点)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com