
| A. | 甲醇 (CH4O) | B. | 甲醛 (CH2O) | C. | 乙醇 (C2H5OH) | D. | 乙酸 (C2H4O2) |
分析 根据质量守恒定律和化合反应的定义和特点判断,主要是利用反应前后原子的种类不变,其数目比保持不变分析判断.
解答 解:“绿色化学”能实现零排放,即反应物中的原子利用率达到100%,也就是说反应类型一般是化合反应,且反应后产物中的各原子数目比不变,CO和H2在一定条件下按照不同的比例反应,可假定反应时的化学计量数之比为m:n,则只要各选项中的化学式能化为形式(CO)m(H2)n,都是正确的.
A、甲醇(CH4O)可变为(CO)1(H2)2,所以正确.
B、甲醛(CH2O)可变为(CO)1(H2)1,所以正确.
C、乙醇 (C2H5OH)不能化为形式(CO)m(H2)n,所以错误.
D、乙酸(C2H4O2)可变为(CO)2(H2)2,所以正确.
故选C.
点评 “绿色化学”的核心是从源头消除污染,实现零排放,即反应物中的原子利用率达到100%,也就是说反应类型一般是化合反应,唯一的生成物即是产品.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 反应前 | 反应后 |  | ||
| A | B | C | D | |
 |  |  |  | |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 金属镁比木炭在空气中燃烧更剧烈------可燃物的性质不同 | |
| B. | 铁丝在空气中不能燃烧,在氧气中能够剧烈燃烧-------氧气含量不同 | |
| C. | 蜂窝煤比煤块在空气中燃烧更剧烈------与氧气接触面积不同 | |
| D. | 火柴头向下比向上放置燃烧个剧烈-------火柴头向上放置与氧气接触面积小 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
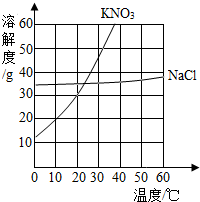 下表是KNO3、NaCl在不同温度下的部分溶解度数据(单位:g/100g水)和二者的曲线,请回答下列问题:
下表是KNO3、NaCl在不同温度下的部分溶解度数据(单位:g/100g水)和二者的曲线,请回答下列问题:| 温度 | 10 | 20 | 40 | 60 | 80 |
| KNO3 | 20.9 | 31.6 | 63.9 | 110 | 169 |
| NaCl | 35.8 | 36 | 36.6 | 37.3 | 38.4 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com