
分析 根据实验室制氧气的操作步骤及注意事项和氧气的性质进行解分析解答本题;根据用排水法收集氧气的合适时机是:气泡连续均匀冒出时收集,以防收集的氧气不纯等进行分析.
解答 解:用高锰酸钾制取氧气时,水槽中的水变红了是因为试管口未塞棉花,高锰酸钾粉末进入水槽;
用排水法收集的氧气不纯的可能的原因是:集气瓶内没有装满水或没等到气泡连续均匀冒出时收集而混有空气;故填:集气瓶内没有装满水或没等到气泡连续均匀冒出时收集;
由于高锰酸钾在加热时能够发生分解产生二氧化锰,这样氯酸钾和高锰酸钾的混合物在受热时高锰酸钾分解产生的二氧化锰就能够对氯酸钾的分解起到催化的作用其中的二氧化锰改变了氯酸钾的分解速率,所以充当催化剂的是二氧化锰,而非高锰酸钾.
答案:没有在试管口放一团棉花,高锰酸钾粉末随氧气流入水中;集气瓶内没有装满水或没等到气泡连续均匀冒出时收集;高锰酸钾分解生成的二氧化锰做催化剂.
点评 化学实验的基本操作是做好化学实验的基础,学生要在平时的练习中多操作,掌握操作要领,使操作规范.


科目:初中化学 来源: 题型:选择题
| A. | 某溶液用pH试纸测试,pH试纸变蓝色(pH约为10),则该溶液一定呈碱性 | |
| B. | 在某溶液中加入氯化钡溶液和稀硝酸,产生白色沉淀,该溶液中一定含有硫酸根离子 | |
| C. | 在某固体物质中加入稀盐酸,产生大量气泡,该物质一定是碳酸盐 | |
| D. | 在稀盐酸与氢氧化钠反应后的溶液中滴加无色酚酞试液不变色,则两者恰好完全反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 化学引领了相关科学与技术的进步 | |
| B. | 粮食、能源、环境三大问题的解决离不开化学 | |
| C. | 化学使人类告别只依赖天然材料、天然药物、天然肥料的时代 | |
| D. | 化学用品在生产制备过程中会产生有害物质,造成环境污染,应抑制化学发展 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 二氧化碳可用来作灭火剂、制泠剂 | |
| B. | 利用固态二氧化碳可以进行人工降雨 | |
| C. | 温室里施用二氧化碳对植物生长不利 | |
| D. | 大气中二氧化碳过多会造成温室效应 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
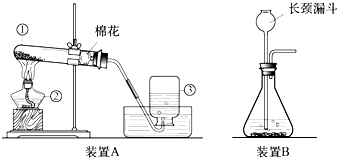
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
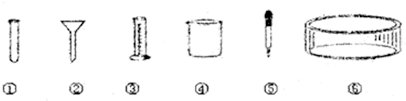
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验步骤 | 实验现象 | 实验结论 | |
| 实验一 | 将带火星的木条伸入装有过氧化氢溶液的试管中 | 有少量气泡 木条不复燃 | 常温下过氧化氢溶液分解速率很慢. |
| 实验二 | 在装有过氧化氢溶液的试管中加入少量Al2O3,然后将带火星的木条伸入试管中 | 产生大量的气泡 木条复燃 | Al2O3能加快过氧化氢的分解速率 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com