
【题目】金属材料在生产、生活中应用广泛。
(1)图A、B、C是金属属的应用实例,根据这些实例可推断出金属具有的物理性质有____________(需答两点)。

(2)图D中,最容易生锈的部位是___________(填“a”“b”或“c”)。
(3)焊锡(主要含锡、铅)与其组成它的纯金属相比具有_______________的特性,可用来焊接金属。
(4)将纯铜片和黄铜片互相刻画画,纯铜片上留下明显的划痕(实验如图E所示),该实验说明了________________________________.
(5)用磁铁矿(Fe3O4)炼铁的原理是:在高温下,用一氧化碳把铁从磁铁矿里还原出来,该反应的化学方程式为_________________。
【答案】 导热性、导电性、延展性 b 熔点低 合金的硬度比其组成它的纯金属大(或黄铜的硬度比纯铜大) 4CO + Fe3O4 ![]() 3Fe + 4CO2
3Fe + 4CO2
【解析】(1)金属用作电缆,是利用了它的导电性;用于制作铁锅,利用的金属的导热性;用于制作金属丝,利用的金属具有延展性;
(2)铁与氧气、水充分接触时容易生锈,在一烧杯中放有一根铁钉,使其一半在液面以上,一半在液面以下,b点铁最容易与氧气、水同时接触,最容易生锈;
(3)合金的熔点比组成它的纯金属的熔点低,焊锡(主要含锡、铅)与其组成它的纯金属相比具有熔点低的性质,可用来焊接金属;
(4)将纯铜片和黄铜片互相刻画,纯铜片上留下明显的划痕,说明合金的硬度比其组成它的纯金属大;
(5)用磁铁矿(Fe3O4)炼铁的原理是:在高温下,用一氧化碳把铁从磁铁矿里还原出来,同时生成二氧化碳,反应的化学方程式为:Fe3O4+4CO![]() 3Fe+4CO2。
3Fe+4CO2。


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】化学是以实验为基础的科学,根据下列实验回答下列问题:

(1)该实验的实验目的是________________________,
(2)当恰好完全反应时锥形瓶中的现象是:________,
(3)图中所示称量的质量是_______g。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】电池是日常必备用品之一,但它也是环境污染的一个重要来源。下面是某兴趣小组利用废旧锌锰干电池作为原料,并进行相关探究的过程。
(知识储备)
(1)锌锰电池的构造和组成(见图)。

(2)结晶水合物的特殊性质:在逐步升高温度条件下,结晶水合物能失去部分或者全部结晶水,如蓝色的胆矾晶体(CuSO4 5H2O)受热时可失去结晶水变为白色的无水硫酸铜粉末(CuSO4)。
I.制备皓矾晶体(ZnSO4xH2O)
小组同学参观了某回收废旧锌锰电池的工厂,其回收工艺流程如图:

(1)流程图中试剂a的化学式是________;得到的滤液1农业上可用作_______________。
(2)将滤渣B在空气中充分灼烧可提纯制得的固体是_________,该方法提纯的原理是(用化学方程式回答)______________________。
(3)测定锌皮(铜芯)中锌的质量分数:称取不同质量锌皮(铜芯)于烧杯中,并加入等浓度的稀硫酸,数据如下表所示:
锌皮(铜芯)的质量 | 20g | 15g |
稀硫酸的质量 | 100g | 120 g |
生成气体的质量 | 0.4 g | 0.4 g |
求:锌皮(铜芯)中锌的质量分数。(写出计算过程,答案保留一位小数)_______
(4)滤液2中溶质主要是硫酸锌,其有关溶解度和温度关系如下表,
温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
溶解度/g | 41.8 | 54.1 | 70.4 | 74.8 | 67.2 | 60.5 |
将滤液2蒸发浓缩、_____________、过滤、洗涤、干燥,可得到皓矾晶体(ZnSO4xH2O)。
小组同学将部分皓矾晶体(ZnSO4xH2O)带回实验室,用如图装置测定晶体中结晶水的含量(图中半透膜可让气体通过又可防止固体粉末进入导管)。测定方法:称取28.7g晶体置于C装置的硬质玻璃管中,加热至完全失去结晶水:

(ZnSO4xH2O ==== ZnSO4 + xH2O),冷却至常温后,称量玻璃管中固体其质量为16.1g。
(5) A中的化学方程式是______________,B中的试剂可从下列物质中选取,你的选择是________。
A.浓硫酸 B.硝酸银溶液 C.饱和碳酸钠溶液 D.澄清石灰水
(6)实验过程中若不通入空气测得的结果将____________
(填“偏大”、 “偏小”或“无影响”)。根据实验结果,计算皓矾晶体中结晶水的x值为_____。
(7)将上述皓矾晶体加热会逐渐失去部分结晶水,加热过程中有关残留固体质量如右图,写出C-D
段发生反应的化学方程式____________________。

查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如下图,在宏观、微观与符号之间建立联系,是化学学科的特点。
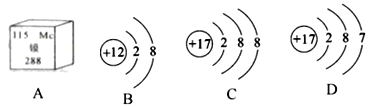
(1)图A所示是近年新命名的元素,其原子核内的质子数是_________。
(2)由B、C两种微粒构成的物质化学式为_____。
汽车尾气在装有催化剂的净化器中反应的微观过程可用下图表示:

(3)该反应中没有发生改变的粒子是 _____________(填“分子”“原子”或“离子”)写出上述反应的化学方程式:________________________。
(4)氮的氧化物是形成酸雨的主要气体之一,可用___________来测定雨水的酸碱度。
查看答案和解析>>
科目:初中化学 来源: 题型:
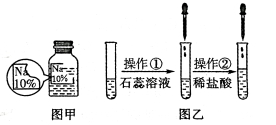
【题目】(7分)某同学在实验室发现了一瓶标签残缺的无色溶液﹙如图甲所示﹚,为确认其中的溶质,他设计并进行了如下探究活动,请回答下列问题。
【猜想与假设】其溶质可能为NaCl、NaOH、Na2CO3和NaHCO3中的一种。
【资料查阅】上述四种物质的相关信息如下:
物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
常温下的溶解度/g | 36 | 109 | 21.5 | 9.6 |
常温下某稀溶液的pH | 7 | 13 | 11 | 9 |
【探究过程】
如图乙所示,在操作①后可确定溶质不是NaCl,则其实验现象应是 ;
在进行操作②时有无色无味得到气体产生,由此又可排除假设物质中的 。
【探究结论】
你认为该溶液中的溶质可能是上述假设物质中的 ,你的判断依据是 。
【探究反思】
(1)若上述探究结论是正确的,操作②产生的气体应是 (写化学式),实验室检验该气体的实验操作及现象是 。
(2)另有同学猜想其中的溶质还可能是Na2SO4,但又没有Na2SO4的上述表列信息。
请你根据以上实验操作的相关现象,判断该溶液中的溶质是否是Na2SO4,并叙述理由: 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学实验中经常用到一定溶质质量分数的溶液。
(1)实验室配制质量分数为4%的氯化钠溶液50g
①需要固体氯化钠的质量_____________g,水___________mL(水的密度1g∕cm3)
②用托盘天平称量所需的氯化钠钠时,移动好游码,向托盘中加入氯化钠,若指针偏向分度盘的左边,要进行的操作是_____________________。
(2)若用质量分数为6%的氯化钠溶液液(密密度约为1.04g/cm3)配制50g质量分数为3%的氯化钠溶液。
①需要6%的氯化钠溶液_________mL(计算结果保留一位小数),水________g。
②该溶液配制过程中除用到量筒、玻璃棒和烧杯外,还需要的仪器是_____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室有一瓶长期暴露在空气中的氢氧化钠固体样品,观察发现,样品表面有白色粉末。某兴趣小组的同学对该样品的成分及含量进行了探究。
(提出问题1)该样品中含有哪些物质?
(提出猜想)猜想Ⅰ:全部是NaOH;
猜想Ⅱ:已完全变质,该样品中只含Na2CO3;
猜想Ⅲ:部分变质,该样品中含有NaOH和Na2CO3。
(实验探究1)为确定该样品成分,小明设计了如下实验方案,请你一起完成下列实验报告。
实验操作 | 实验现象 | 实验结论 |
①取少量样品溶于水,加入 足量的________; | 白色沉淀产生 | 该反应的化学方程式为 ________ |
②将上述反应后的混合液过滤, 取滤液加入________; | ________ | 证明猜想Ⅲ成立 |
(提出问题2)怎样提纯该样品得到纯净的氢氧化钠固体?
(实验探究2)为得到纯净的氢氧化钠固体,设计的实验过程如下图。请回答下列问题

⑴长期暴露在空气中的氢氧化钠固体样品极易变质,原因是________(用化学方程式表示)。操作B的名称为________,所需的玻璃仪器有________、烧杯和玻璃棒。
⑵该实验中发生反应的化学方程式为________。
⑶最终所得氢氧化钠固体质量________(选填“<”、“=”或“>”)变质后样品中氢氧化钠的质量。
(实验探究3)为了测定NaOH的纯度,某同学设计如图装置。
已知:CO2在饱和碳酸氢钠溶液中几乎不溶解。

⑷B中集气瓶盛放的饱和碳酸氢钠溶液不能用水代替,其理由是________。
⑸取10g样品进行实验,根据实验数据,通过计算可知产生了CO20.44g,求原样品中NaOH的质量分数,写出计算过程_____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是甲、乙两种不含结晶水的固体物质的溶解度曲线。
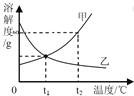
根据图示判断,下列有关说法中,不正确的是:( )
A. 在t1℃时,甲物质的饱和溶液升温到t2℃时,溶液不变浓
B. 将t1℃时,乙物质的饱和溶液升温,会析出晶体
C. 在t2℃时,160g甲物质的饱和溶液中含有甲60g
D. 在t2℃时,乙溶液的溶质质量分数小于甲溶液的溶质质量分数
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】利用下图装置进行实验。实验前K1、K2均已关闭。
实验装置 | 实验1 | 实验2 |
| Ⅰ. A中盛有水,液面浸没下端导管口,B中盛有含酚酞的NaOH溶液 Ⅱ.将注射器中的浓硫酸注入A中,并保持注射器活塞不动,充分接触后,打开K1和K2 | Ⅰ. A中充满CO2,B中盛有一定量的水 Ⅱ. 将注射器中的NaOH溶液(足量)注入A中,充分反应后,打开K1和K2 |
(1)检查A装置气密性:向下推注射器的活塞,松手后活塞恢复至原位,该现象说明________。
(2)实验1观察到A中液体流入B中,B中溶液由红色变成无色,产生该现象的原因是_________。
(3)实验2不能证明二氧化碳与氢氧化钠发生反应,其理由是_________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com