
| 序号 | A | B | C | D |
| 实验 | 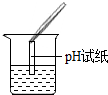 | 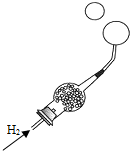 | 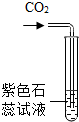 | 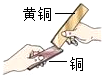 |
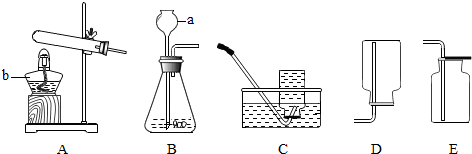
| 实验目的 | 检测溶液的酸碱性 | 验证氢气密度小于空气 | 验证二氧化碳溶于水显酸性 | 相互刻划比较合金与纯金属的硬度大小 |
| A. | A | B. | B | C. | C | D. | D |
分析 A、根据pH试纸的使用注意事项分析;
B、根据氢气的密度结合实验现象分析;
C、根据二氧化碳和水反应产生碳酸显酸性,酸性溶液能使石蕊试液变成红色分析;
D、根据合金的特性解答.
解答 解:A、pH试纸测定溶液的pH时,不能浸入试剂内,故操作错误;
B、氢气的密度比空气小,吹气泡时气泡会上升,故操作正确;
C、二氧化碳和水反应产生碳酸显酸性,酸性溶液能使石蕊试液变成红色,故操作正确;
D、合金的特性是硬度大,熔点低,故通过刻划可以比较黄铜和铜的硬度,故操作正确;
故选项为:A.
点评 本题考查化学实验方案的评价,为高频考点,侧重实验基本操作和实验技能的考查,注意实验操作的评价性分析,题目难度不大.


科目:初中化学 来源: 题型:选择题
| A. | 水能溶解所有的物质 | B. | 长期饮用硬水不利于身体健康 | ||
| C. | 我国淡水资源丰富,不需节约 | D. | 通过过滤可将海水淡化 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 溶剂的质量蒸发掉一半 | |
| B. | 溶质的质量增加一倍 | |
| C. | 蒸发掉的溶剂质量等于溶液质量的一半 | |
| D. | 加入100克溶质质量分数为10%的此溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
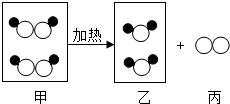 如图是某反应的微观示意图,若○表示氧原子,●表示氢原子,有关说法正确的是( )
如图是某反应的微观示意图,若○表示氧原子,●表示氢原子,有关说法正确的是( )| A. | 图中甲、乙、丙三种物质都是氧化物 | |
| B. | 图中甲、乙、丙三种物质均是由分子构成的 | |
| C. | 反应前后分子种类、原子种类均没有改变 | |
| D. | 该反应属于置换反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
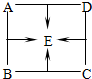 A、B、C、D、E为单质和氧化物中的五种物质,它们有如图所示关系.已知其中A、B、E为氧化物,且A与B反应、B与C反应均生成一种红色物质.请你根据图示和所给条件回答下列问题:
A、B、C、D、E为单质和氧化物中的五种物质,它们有如图所示关系.已知其中A、B、E为氧化物,且A与B反应、B与C反应均生成一种红色物质.请你根据图示和所给条件回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 实验室中,常采用分解过氧化氢溶液(二氧化锰作催化剂)或加热高锰酸钾的方法制取氧气.
实验室中,常采用分解过氧化氢溶液(二氧化锰作催化剂)或加热高锰酸钾的方法制取氧气.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com