
| 物 质 | Cr | Mg | Ag |
| 实验现象 | 产生气泡速度缓慢 | 产生气泡速度快 | 无任何现象 |
| 操作 | 将Ag片放入氯化铬溶液中 | 将铬放入氯化镁溶液中 |
| 现象 | 无明显现象 | 无明显现象 |
| 结论 | Cr>Ag | Mg>Cr |
分析 根据已有的知识进行分析解答,在金属活动性顺序中,氢前的金属能与酸反应产生氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,据此解答.
解答 解:根据三种金属中镁的活动性强于银,还可以猜想为:Mg>Cr>Ag;故填:Mg>Cr>Ag;
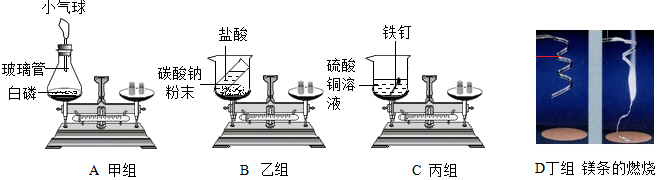
(1)三种金属加入盐酸前都先用砂纸将表面擦光亮,是为了除去表面的氧化物,故填:除去表面的氧化物.
(2)铬在盐酸中缓慢产生气泡,镁在盐酸中产生气泡速度快,说明镁和铬在氢前,且镁的活动性强于铬,银在盐酸中无任何现象,说明银在氢后,故金属活动性顺序为Mg>Cr>Ag,故猜想b正确,故填:b;
(3)还可以利用金属与盐溶液是否反应验证金属的活动性顺序,故可以将银放入氯化铬溶液中,无现象,说明铬的活动性强于银,将铬放入氯化镁溶液中没有现象,说明镁的活动性强于铬,故填:
| 操作 | 将Ag片放入 氯化铬溶液中 | 将 铬放入 氯化镁溶液中 |
| 现象 | 无明显现象 | 无明显现象 |
| 结论 | Cr>Ag | Mg>Cr |
点评 本题考查的是金属活动性顺序的探究,完成此题,可以依据已有的金属活动性顺序的意义进行.


 智能训练练测考系列答案
智能训练练测考系列答案科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

| 步骤 | 操作 | 现 象 | 结 论 |
| ① | 取少量滤液B于试管中,再滴加足量的CaCl2溶液溶液 | 如果观察到无沉淀 | 则猜想①成立. |
| 如果观察到有沉淀, | 则猜想②或③成立 |
| 步骤 | 操作 | 现 象 | 结 论 |
| ② | 取少量清液于试管中,加入足量的盐酸 | 整个实验过程无气泡产生 | 说明滤液B中无未反应完的NaHCO3 |
| ③ | 取少量清液于试管中,加入酚酞试液 | 如果观察到溶液变红色, | 则猜想③成立 |
| 如果无明显现象 | 则猜想②成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 步骤 | 现象 | 结论 |
| ①取1.8g红色固体于试管中,滴加足量稀硫酸,充分反应 | 溶液由无色变蓝色 | 猜想①错误 |
| ②过滤,将滤渣洗涤、干燥、称量 | 所得固体质量大于0.8g | 猜想③正确 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com