
【题目】化学学习小组用金属镁进行实验探究.
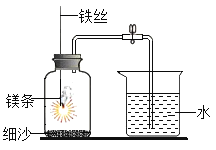
(1)甲同学利用如图装置进行空气里氧气含量的实验,待镁条燃烧完全并冷却后打开止水夹,发现进入集气瓶中水的体积约占集气瓶容积的70%.
①正常情况下,如果镁条只和空气中的氧气反应,则进入集气瓶中水的体积最多不超过其容积的_____.根据空气的组成同学们推出减少的气体为氧气和_____.
②下列是同学们对“测定空气里氧气的含量”实验的认识,其中错误的是_____(填选项字母代号)
A 装置不漏气是实验成功的重要因素之一 B 可燃物用量不足会影响实验结论
C 瓶内气压变小能将水吸入集气瓶内 D 燃烧结束后应立即进行测量
(2)乙同学将燃着的镁条插入盛有二氧化碳的集气瓶中,发现镁条继续燃烧,集气瓶壁上有黑色固体和白色固体产生,请写出该反应的化学方程式_____.分析实验(1)、(2),你对燃烧有了哪些新的认识?_____(写出一条即可)
(3)丙同学将镁条插入硝酸铜、硝酸锌的混合溶液中,充分反应后过滤,向滤渣中滴加稀盐酸,发现有气泡产生,则滤渣中一定含有_____,滤液中一定含有的金属离子是_____.
(4)丁同学将3.6g镁带放入100g稀硫酸中,正好完全反应,试计算该硫酸溶液的溶质质量分数._____
【答案】![]() 氮气 D
氮气 D ![]() 燃烧不一定需要氧气的参与 铜,锌 镁离子(符号也可) 14.7%
燃烧不一定需要氧气的参与 铜,锌 镁离子(符号也可) 14.7%
【解析】
(1)空气成分测定中已知氧气是占空气体积的五分之一,而用镁条做该实验测得的结果是70%,说明镁条和空气中的其他成分而其他成分中能达到如此比例的也只有氮气,所以可以推测应该是和氧气、氮气发生了反应;
(2)根据(1)(2)信息可推知燃烧不一定都需要氧气参与;
(3)涉及金属的活动性由强到弱的顺序镁、锌、铜,同时按照金属反应的优先原则,镁先和硝酸铜反应,待硝酸铜完全反应后才和硝酸锌反应,而滤渣滴加盐酸有气体,说明一定有生成的锌,还有可能同时存在剩余的镁,进而推测对应的离子;
(4)根据镁条的质量和对应的化学方程式求算对应的稀硫酸中溶质的质量,进而求算其质量分数。
(1)空气成分测定中已知氧气是占空气体积的五分之一,而用镁条做该实验测得的结果是70%,说明镁条和空气中的其他成分而其他成分中能达到如此比例的也只有氮气,所以可以推测应该是和氧气、氮气发生了反应;所以
①正常情况下,如果镁条只和空气中的氧气反应,则进入集气瓶中水的体积最多不超过其容积的![]() ,根据空气的组成同学们推出减少的气体为氧气和氮气。
,根据空气的组成同学们推出减少的气体为氧气和氮气。
②A、装置不漏气是实验成功的重要因素之一,这样才能保证水的等量代换,正确;
B、可燃物用量不足会影响实验结论,可燃物不足,会导致装置内的能消耗的气体不能被完全消耗,进而影响实验结论,正确;
C、该实验的原理就是利用瓶内气压变小能将水吸入集气瓶内,进而等量替代,正确;
D、由于该反应放热,而气体的体积收到温度的影响,所以实验结束后应该等装置恢复到室温打开止水夹进而读数,否则影响实验结果,错误;
故选:D。
(2)将燃着的镁条插入盛有二氧化碳的集气瓶中,发现镁条继续燃烧,集气瓶壁上有黑色固体和白色固体产生,根据质量守恒定律和物质的颜色状态可知,生成黑色物质为碳,白色固体为氧化镁,对应的化学方程式为![]() ,根据该反应以及(1)可以看出燃烧不一定需要氧气的参与。
,根据该反应以及(1)可以看出燃烧不一定需要氧气的参与。
(3)涉及金属的活动性由强到弱的顺序镁、锌、铜,同时按照金属反应的优先原则,镁先和硝酸铜反应,待硝酸铜完全反应后才和硝酸锌反应,而滤渣滴加盐酸有气体,说明一定有生成的锌,还有可能同时存在剩余的镁,所以滤渣中一定含有生成的铜和锌,可能含有剩余的镁,而滤液中一定存在金属离子是镁离子。
(4)设3.6g镁条完全反应消耗的稀硫酸中的溶质的质量为x,则

![]() ,x=14.7g;
,x=14.7g;
该硫酸溶液的溶质质量分数为![]() 。
。


科目:初中化学 来源: 题型:
【题目】金属在生产和生活中有着广泛应用。
(1)下列金属制品在应用中,利用金属导热性的是_____
a.金属硬币 b.铜制火锅 c.铝制导线
(2)铝比铁活泼,但铝在空气中比铁稳定,其原因是_____
(3)工业上用盐酸除去钢板表面上的锈要严格控制盐酸的用量,用量过多会发生反应而损坏钢板,用化学方程式表示损坏钢板的反应_____
(4)高铁的迅速发展对钢轨的需求量越来越大,质量要求越来越高。工业上经常用“铝热反应”来焊接钢轨,其原理是:![]() ,该反应的基本类型是_____反应;若焊接钢轨需要50.4kg铁,理论上需要铝的质量是_____kg
,该反应的基本类型是_____反应;若焊接钢轨需要50.4kg铁,理论上需要铝的质量是_____kg
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙两种固体的溶解度曲线如图所示。下列说法中正确的是( )
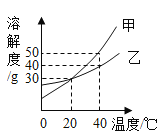
A.![]() 时,100g甲的饱和溶液中含有溶质质量为30g
时,100g甲的饱和溶液中含有溶质质量为30g
B.![]() 时,甲溶液中溶质的质量分数一定大于乙溶液
时,甲溶液中溶质的质量分数一定大于乙溶液
C.![]() 时,甲的饱和溶液中,溶质与溶剂质量比为1:1
时,甲的饱和溶液中,溶质与溶剂质量比为1:1
D.![]() 时,分别在100g水中加入40g甲、乙,加热到
时,分别在100g水中加入40g甲、乙,加热到![]() 时,甲溶液为不饱和溶液
时,甲溶液为不饱和溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学兴趣小组的同学取10 g某锌样品(含少量杂质,且杂质不溶于水,也不与酸反应)于烧杯中,向其中加入一定量的稀硫酸,当加入稀硫酸的质量为93.7 g时,恰好完全反应,生成气体的质量与反应时间的关系如下图所示,试回答下列问题:
(1)完全反应后生成氢气的质量为 g。
(2)样品中锌的质量为多少克?
(3)反应后,所得溶液中硫酸锌的质量分数
为多少?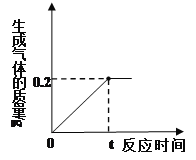
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示是化学实验中常见的基本操作。据图回答下列问题。
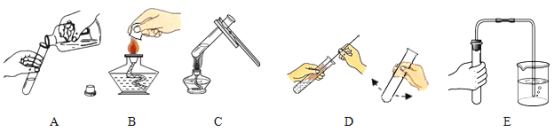
(1)如图A所示,手握细口瓶倾倒液体时,细口瓶标签的一面要________,细口瓶的塞子要在桌面上___________。
(2)如图B所示,用完酒精灯后,必须用__________盖灭,此外,使用酒精灯时,绝对禁止______________(写出一条)。
(3)如图C所示,用酒精灯加热试管里的液体时,应注意:试管外壁应该_________,试管口不要对着____________。
(4)如图E所示,如何检查装置的气密性_________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】现有含HCl和CuCl2的混合溶液50g,向该溶液中逐滴加入溶质质量分数为10%的NaOH溶液,生成沉淀的质量与加入NaOH溶液的质量关系如图所示.
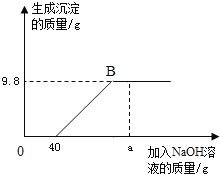
(1)当加入NaOH溶液质量为ag时,溶液中的溶质有____________;
(2)求混合溶液中CuCl2的质量分数_______________.
(3)求恰好完全反应时,消耗NaOH溶液的总质量_________________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硫酸氢的转化是资源利用和环境保护的重要研究课题,将H2S和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应用以回收S,其物质转化如图所示。
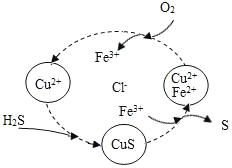
(1)反应中当有34g H2S转化为硫单质时,保持溶液中Fe3+的物质的量不变,需消耗O2的质量为_____。
(2)在温度一定和不补加溶液的条件下,缓慢通入混合气体,并充分搅拌。欲使生成的硫单质中不含CuS,可采取的措施是_____
(3)写出图中各步转化的化学方程式:_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】除去下列物质中混有的少量杂质(括号内为杂质),所用方法错误的是
A. ![]() 通过足量的碳酸氢钠溶液、干燥
通过足量的碳酸氢钠溶液、干燥
B. CaO固体(![]() )固体)--高温充分煅烧
)固体)--高温充分煅烧
C. NaCl固体(泥沙)--加人足量的水溶解、过滤、蒸发结晶
D. KCl溶液(![]() )溶液)--滴加氯化钡溶液至恰好完全反应,过滤
)溶液)--滴加氯化钡溶液至恰好完全反应,过滤
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】有机物X的分子模型如图所示,图中每个“●”代表一个碳原子,每个“○”代表一个氢原子.下列说法中不正确的是( )
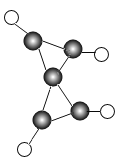
A.X的化学式为C5H4
B.X的相对分子质量是64
C.X分子中碳原子与氢原子的个数比是5:4
D.X在氧气中完全燃烧的产物是CO2、H2O和NO
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com