

分析 (1)玻璃棒用途有搅拌、引流、转移物质等;
溶解粗盐时所加水的质量过多时,蒸发时浪费燃料并且耗时长,也不宜过少,过少时会导致氯化钠不能完全溶解;
(2)氧化钙和水反应生成氢氧化钙,氢氧化钙能和氯化镁反应生成氢氧化镁沉淀和氯化钙,氢氧化钡和氯化镁反应生成氢氧化镁沉淀和氯化钡,氢氧化钠和氯化镁反应生成氢氧化镁沉淀和氯化钠,氢氧化钾和氢氧化镁反应生成氢氧化镁沉淀和氯化钾,和稀盐酸反应生成氯化钾和水;
(3)氯化钡溶液和碳酸钠溶液的添加顺序颠倒时,会导致过量的氯化钡不能除去;
(4)滤液B中含有过量的碱,碱溶液和碳酸钠溶液都是显碱性溶液,都能使酚酞试液变红色;
碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳;
碳酸钠和氯化钡反应生成碳酸钡沉淀和氯化钠;
(5)步骤④中,发生的中和反应是氢氧化钠和稀盐酸反应生成氯化钠和水;
(6)铜不能和稀盐酸反应;
稀盐酸显酸性,pH小于7;
稀盐酸显酸性,不能使酚酞试液变色;
氯离子能和银离子结合生成氯化银沉淀;
(7)反应过程中生成了氯化钠.
解答 解:(1)步骤①中玻璃棒的作用是加快溶解速率;
溶解粗盐时所加水的质量不宜过多,也不宜过少,过多时,蒸发时浪费燃料并且耗时长,也不宜过少,过少时会导致氯化钠不能完全溶解,导致精盐的产率偏低.
故填:加快溶解速率;蒸发时浪费燃料并且耗时长;偏低.
(2)A、氧化钙和水反应生成氢氧化钙,氢氧化钙能和氯化镁反应生成氢氧化镁沉淀和氯化钙,因此X可以是氧化钙;
B、氢氧化钡和氯化镁反应生成氢氧化镁沉淀和氯化钡,因此X可以是氢氧化钡溶液;
C、氢氧化钠和氯化镁反应生成氢氧化镁沉淀和氯化钠,因此X可以是氢氧化钠溶液;
D、氢氧化钙能和氯化镁反应生成氢氧化镁沉淀和氯化钙,因此X可以是氢氧化钙溶液;
E、氢氧化钾和氢氧化镁反应生成氢氧化镁沉淀和氯化钾,和稀盐酸反应生成氯化钾和水,X是氢氧化钾溶液时会带入杂质氯化钾,因此X不能是氢氧化钾溶液.
故填:ABCD.
(3)氯化钡溶液和碳酸钠溶液的添加顺序不能颠倒,这是因为颠倒后不能除去过量的氯化钡;
沉淀B中的成分是BaSO4、CaCO3和BaCO3、Mg(OH)2.
故填:不能;BaCO3、Mg(OH)2.
(4)A、取少量滤液B,滴加酚酞,若变为红色,不能说明Na2CO3过量,这是因为溶液中含有氢氧化钠,氢氧化钠溶液能使酚酞试液变红色;
B、取少量滤液B,滴加足量稀盐酸,若有气泡产生,说明Na2CO3过量;
C、取少量滤液B,滴加氯化钡溶液,若有白色沉淀产生,说明Na2CO3过量.
故填:BC.
(5)步骤④中发生的中和反应是:氢氧化钠和稀盐酸反应生成氯化钠和水,反应的化学反应方程式为:NaOH+HCl═NaCl+H2O.
故填:NaOH+HCl═NaCl+H2O.
(6)A、取样,加入铜,若无现象,不能说明盐酸没有剩余,这是因为铜不能和稀盐酸反应;
B、取样,测溶液pH,若pH<7,说明盐酸有剩余;
C、取样,加碳酸钠溶液,若有气泡产生,说明有盐酸剩余;
D、取样,滴入酚酞溶液,若溶液呈无色,不能说明盐酸没有剩余,这是因为盐酸显酸性,不能使酚酞试液变色;
E、取样,加硝酸银溶液,若有白色沉淀产生,不能说明有盐酸剩余,这是因为氯化钠能和硝酸银反应生成白色沉淀氯化银.
故填:BC.
(7)该方案实际得到的氯化钠比原粗盐中含有的氯化钠要多,是因为反应生成了氯化钠.
故填:反应生成了氯化钠.
点评 加入碳酸钠溶液、氢氧化钠溶液(或其它溶液)和氯化钡溶液除去杂质时,碳酸钠溶液应该在加入氯化钡溶液后再加入,否则过量的氯化钡溶液无法除去.


 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:初中化学 来源: 题型:解答题
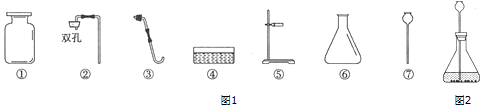
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
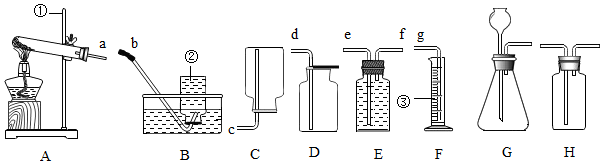
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
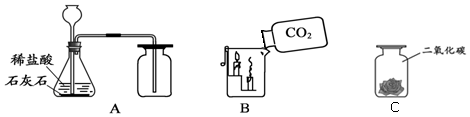
查看答案和解析>>
科目:初中化学 来源: 题型:计算题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com