
| 实验序号 | 所用试剂 | 现象及结论 |
| A | 酚酞溶液 | 溶液为无色,一定恰好中和 |
| B | pH试纸 | 测得pH>7,则氢氧化钠溶液过量 |
| C | 铁粉 | 有气泡产生,则稀盐酸过量 |
| D | 氯化铜溶液 | 没有蓝色沉淀,一定恰好中和 |
| A. | A | B. | B | C. | C | D. | D |
科目:初中化学 来源: 题型:实验探究题
| 实验步骤 | 观察到的现象 |
| A.在试管中取少量稀硫酸,插入足量的铁棒,充分作用. | ①产生气泡,溶液变成浅绿色 |
| B.在A所得的溶液中插入足量的②银棒,充分作用. | 无明显现象 |
| C.在B所得的溶液中插入足量的③铝棒,充分作用. | 该金属棒上附着黑色物质,溶液由浅绿色变为无色 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 大力发展煤炭发电以缓解煤炭产能过剩问题 | |
| B. | 积极植树造林 | |
| C. | 用清洁能源代替化石燃料 | |
| D. | 禁止焚烧农作物秸秆和垃圾 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
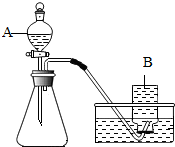 某兴趣小组根据实验室提供的仪器和药品进行了氧气的制备实验.
某兴趣小组根据实验室提供的仪器和药品进行了氧气的制备实验.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
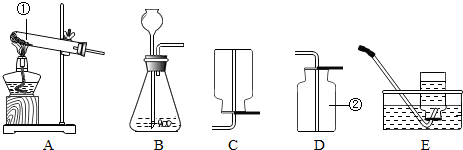
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | N>M>X>Y | B. | Y>X>M>N | C. | X>Y>M>N | D. | N>M>Y>X |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①②③ | B. | ①②④ | C. | ①③④ | D. | ②③④ |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
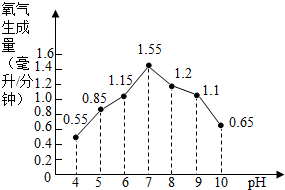 实验室常以MnO2为催化剂分解H2O2制取氧气,小柯在科普读物中查得一些蔬菜提取液也可催化H2O2分解,为此,他设计并进行了如下实验:
实验室常以MnO2为催化剂分解H2O2制取氧气,小柯在科普读物中查得一些蔬菜提取液也可催化H2O2分解,为此,他设计并进行了如下实验:| 蔬菜 名称 | 每分钟氧气生成量 (毫升/分钟) |
| 莴笋 | 1.55 |
| 白菜 | 0.7 |
| 菠菜 | 0.9 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com