
科目:初中化学 来源: 题型:解答题

| 物质 | Ca(ClO3)2 | CaCl2 | KClO3 | KCl |
| 溶解度/g | 209.0 | 74.5 | 7.3 | 34.2 |

查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
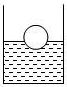 化学就在我们身边,与我们的生活息息相关.请回答以下生活中的问题:
化学就在我们身边,与我们的生活息息相关.请回答以下生活中的问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 某化学小组利用下图所示装置测定铜锌合金样品中锌的质量分数(图中固定装置已略去)
某化学小组利用下图所示装置测定铜锌合金样品中锌的质量分数(图中固定装置已略去)查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 我国水资源十分充足,但人均占有量低 | |
| B. | 地球上储水量最大的是河流水 | |
| C. | 水是人类宝贵的自然资源 | |
| D. | 水资源不足,将导致严重的社会危机 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com