
分析 在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和.所以质量守恒定律只能用来解释化学反应,可以据此解答
解答 解:根据质量守恒定律,铁丝在氧气中点燃燃烧生成的四氧化三铁的质量等于铁的质量与参加反应的氧气的质量之和,故比铁丝的质量增加了;
根据质量守恒定律,被分解的高锰酸钾的质量等于剩余固体和生成的氧气的质量之和,氧气扩散到空气中,因此加热高锰酸钾后留下的固体物质的质量比高锰酸钾的质量小.
这两种现象都可以用质量守恒定律来解释.
答:根据质量守恒定律,铁丝在氧气中点燃燃烧生成的四氧化三铁的质量等于铁的质量与参加反应的氧气的质量之和,故比铁丝的质量增加了;
根据质量守恒定律,被分解的高锰酸钾的质量等于剩余固体和生成的氧气的质量之和,氧气扩散到空气中,因此加热高锰酸钾后留下的固体物质的质量比高锰酸钾的质量小.
质量守恒定律.
点评 本题主要考查学生对质量守恒定律的认识和灵活运用这一定律解答问题的能力,质量守恒定律适用于所有的化学变化.


 应用题作业本系列答案
应用题作业本系列答案科目:初中化学 来源: 题型:选择题
| A. | 空气中含量最多的单质是氮气 | |
| B. | 按目前测定,海水中含量最多的元素是氧元素 | |
| C. | 煤、石油、沼气、风能等都是可再生能源 | |
| D. | 防止金属腐蚀是保护金属资源的有效途径 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氮气可用作保护气,说明氮气不与任何物质发生反应 | |
| B. | 做硫在氧气中燃烧实验时,在集气瓶中留少量水可吸收二氧化硫 | |
| C. | 氧气易溶于水,可以供给水中植物呼吸 | |
| D. | 常用带火星的木条检验空气中的氧气 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
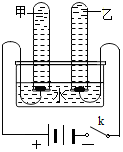 (1)水在自然环境中不易分解,但在通电的条件下可以分解,写出该反应的化学方程式2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,在如图所示的装置中,当通电一段时间后,甲管中气体的体积与乙管中气体的体积之比为1:2.
(1)水在自然环境中不易分解,但在通电的条件下可以分解,写出该反应的化学方程式2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,在如图所示的装置中,当通电一段时间后,甲管中气体的体积与乙管中气体的体积之比为1:2.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
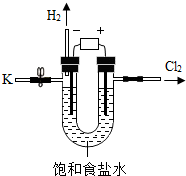 某学习小组对课本中“食盐常用于制氧气、烧碱”的内容产生兴趣.在老师的指导下,用自制的实验装置(主要部分如图所示)进行电解饱和食盐水制取氢氧化钠的实验.一段时间后,关闭电源,从K处导出部分的溶液作为待测液进行如下研究.
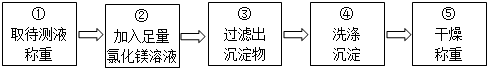
某学习小组对课本中“食盐常用于制氧气、烧碱”的内容产生兴趣.在老师的指导下,用自制的实验装置(主要部分如图所示)进行电解饱和食盐水制取氢氧化钠的实验.一段时间后,关闭电源,从K处导出部分的溶液作为待测液进行如下研究.| 实验步骤 | 实验现象 | 实验结论 |
| 待测液呈碱性,表明含有氢氧化钠. |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
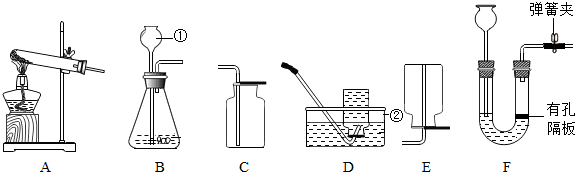
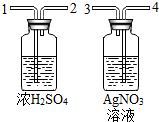
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| KNO3 | 13.3 | 20.9 | 32 | 45.8 | 64 | 85.5 | 110 | 138 | 169 | 202 | 246 |
| NaCl | 35.7 | 35.8 | 36 | 36.3 | 36.6 | 37 | 37.3 | 37.8 | 38.4 | 39 | 39.8 |

| 资料:A的溶解度 | |||||
| 温度/℃ | 20 | 30 | 40 | 50 | 60 |
| 溶解度/g | 37.2 | 41.4 | 45.8 | 50.4 | 55.2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com