

分析 (1)据常用仪器回答;
(2)实验室利用加热高锰酸钾制取氧气不需加入催化剂,实验室制取二氧化碳用大理石和稀盐酸,据反应原理书写方程式,二氧化碳能溶于水,故一般不用排水法收集;检验二氧化碳的性质时,气体要从长管进入,与溶液充分接触,二氧化碳和水反应生成碳酸,碳酸可使石蕊变红;
(3)据实验现象回答;
(4)要减缓反应速率,可控制反应物的量或反应物溶液的浓度;
(5)浓硫酸是液体,所以不能用B装置,液体会流出,据反应原理书写方程式.
解答 解:(1)标号仪器分别是铁架台和酒精灯;
(2)实验室利用加热高锰酸钾制取氧气不需加入催化剂,反应属于固体加热型,故选发生装置B;实验室制取二氧化碳用大理石和稀盐酸,反应生成氯化钙、水和二氧化碳,反应方程式是CaCO3+2HCl=CaCl2+H2O+CO2↑;二氧化碳能溶于水,故一般不用排水法收集;检验二氧化碳的性质时,气体要从长管进入,与溶液充分接触,且若先通入G,则气体无法排出,则无法观察其通入E后的现象,二氧化碳和水反应生成碳酸,碳酸可使石蕊变红;
(3)向烧杯中慢慢倾倒CO2,发现下层的蜡烛先熄灭,上层蜡烛后熄灭,说明CO2具有不能燃烧、不能助燃的化学性质;
(4)要减缓反应速率,可控制反应物的量或反应物溶液的浓度;
a、用容积较小的锥形瓶,反应生成的较多气体无法排出,不安全;
b、将长颈漏斗换成针筒减慢液体的滴加速度,从而可控制反应速率,可行;
c、加热反应物,反应速率加快,生成气体增多,更不安全;
d、降低液体反应物的浓度,中溶质的质量减小,可减缓反应速率,可行;
(5)浓硫酸是液体,所以不能用B装置,试管口向下,液体会流出,加热氯化钠固体与浓硫酸的混合物的方法来制取氯化氢气体,属于酸和盐的反应是复分解反应,据复分解反应化合物互换成分的特点,同时生成硫酸钠,反应方程式是:2NaCl+H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$Na2SO4+2HCl↑;
故答案为:
(1)铁架台; 酒精灯
(2)B; CaCO3+2HCl=CaCl2+H2O+CO2↑;二氧化碳能溶于水; F; 石蕊试液变红;
(3)不能燃烧或不支持燃烧;
(4)b、d;
(5)不能; 2NaCl+H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$Na2SO4+2HCl↑.
点评 本题较为综合的考查了实验室制取气体的发生和收集装置的选取,据反应物状态和反应条件选择发生装置,并考查了制取气体的反应原理、二氧化碳的性质等知识,掌握相关知识才能结合选项正确解答.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:选择题
| A. | 铝是地壳中含量最多的金属元素 | |
| B. | 生活中广泛使用的铁制品大多数是铁合金 | |
| C. | 用铁丝、Al2(SO4)3溶液、CuSO4溶液能推断出铝、铁、铜的活动性顺序 | |
| D. | 人类最早冶炼和使用的金属是铝 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验内容 | 实验现象 | 分析与结论 |
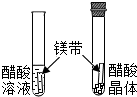 | 装有醋酸晶体试管内没有气泡冒出,装有醋酸溶液试管中镁带表面冒气泡. | 酸的很多反应通常在水溶液中才能完成. |
用玻璃棒蘸硫酸在白纸上写字 | 浓(填“浓”或“稀”)硫酸使白纸炭化. | 即使是同种酸,由于浓度不同,它们的性质不完全相同. |
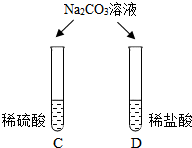 | 两试管中均产生气泡 | 不同的酸具有相似的性质,这是因为酸的溶液中都含有H+(填化学符号). |
 | E试管中产生白色沉淀, F试管中无明显现象. | 不同的酸根会导致酸的“个性”差异.因此,可用氯化钡溶液鉴别盐酸和硫酸. |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
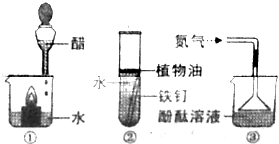
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| 选项 | 物质 | 杂质 | 试剂 | 操作方法 |
| A | 碳粉 | 铁粉 | 适量硫酸铜溶液 | 反应后过滤 |
| B | 稀盐酸 | 硫酸 | 适量氢氧化钡溶液 | 滴加 |
| C | 氮气 | 水蒸气 | 浓硫酸 | 用浓硫酸洗气 |
| D | 生石灰 | 碳酸钙 | 过量稀盐酸 | 蒸发 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A.生活常识 | B.物质鉴别 |
| 硬水与软水--观察颜色区别 人体缺钙元素--导致甲状腺肿大 | 食盐与亚硝酸钠--品尝味道 硝酸铵和磷矿粉(不溶于水)--加水溶解 |
| C.安全常识 | D.“一定”与“不一定” |
| 长时间堆放的柴草--要不时翻动 进入陌生溶洞--先做灯火实验 | 有盐和水生成的反应一定是中和反应 不饱和溶液转化为饱和溶液,溶质质量分数一定变大 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com