
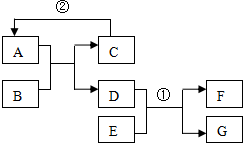
 已知A-G均为初中化学常见的物质.其中A、C是组成元素相同的气体,且C能产生温室效应,B是赤铁矿的主要成分,F为紫红色,E可用于配制农药波尔多液.根据如图所示的转化关系(图中反应条件均已略去),请回答:
已知A-G均为初中化学常见的物质.其中A、C是组成元素相同的气体,且C能产生温室效应,B是赤铁矿的主要成分,F为紫红色,E可用于配制农药波尔多液.根据如图所示的转化关系(图中反应条件均已略去),请回答:分析 根据题目中的突破口“A、C是组成元素相同的气体,且C能产生温室效应”、“B为红棕色,是赤铁矿的主要成分”、“F是紫红色金属;E可用于配制农药波尔多液”,则C是二氧化碳,A是一氧化碳;B为红棕色,是赤铁矿的主要成分,所以B是氧化铁;F是紫色金属属于铜,E可用于配制农药波尔多液是硫酸铜,再进一步进行分析即可.
解答 解:根据题目中的突破口“A、C是组成元素相同的气体,且C能产生温室效应”、“B是赤铁矿的主要成分”、“F是紫红色金属;E可用于配制农药波尔多液”,则C是二氧化碳,A是一氧化碳;B为红棕色,是赤铁矿的主要成分,所以B是氧化铁;F是紫色金属属于铜,E可用于配制农药波尔多液是硫酸铜.代入检验,符合题意.则:
(1)根据分析,B是氧化铁,C是二氧化碳,故其化学式分别为Fe2O3;CO2;
(2)根据分析,反应①铁和硫酸铜反应生成铜和硫酸亚铁,化学方程式是:Fe+CuSO4═Cu+FeSO4;
(3)反应②是二氧化碳在高温条件下与炭反应,生成一氧化碳,是两种物质相反应生成一种新的物质的反应类型,属于化合反应,是吸热反应.
故答案为:
(1)Fe2O3 CO2 (2)Fe+CuSO4═FeSO4+Cu
(3)化合反应 吸热
点评 解答本题关键是要找出突破口,知道造成温室效应的主要气体是二氧化碳,赤铁矿的主要成分是氧化铁,紫色金属是铜,蓝色沉淀是氢氧化铜,再根据学过去的知识进一步进行分析推断即可.


科目:初中化学 来源: 题型:选择题
| A. | H2SO4、Na2O、MgCl2、Ca(OH)2 | B. | Na2CO3、Ba(OH)2、Na2O、H2SO4 | ||
| C. | HNO3、KOH、Na2CO3、CaO | D. | H2SO4、CaCO3、KOH、SO2 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| Fe3O4 | Fe2O3 | 铁 | |
| 分解温度/℃ | 1538 | 1400 | / |
| 熔点/℃ | / | / | 1535 |
| A. | 铁丝在氧气里燃烧时产生火星四射现象 | |
| B. | 可以用稀盐酸验证球状物质中含有铁 | |
| C. | 铁丝燃烧时温度高于1400℃而低于1535℃ | |
| D. | Fe3O4中铁元素具有两种化合价 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
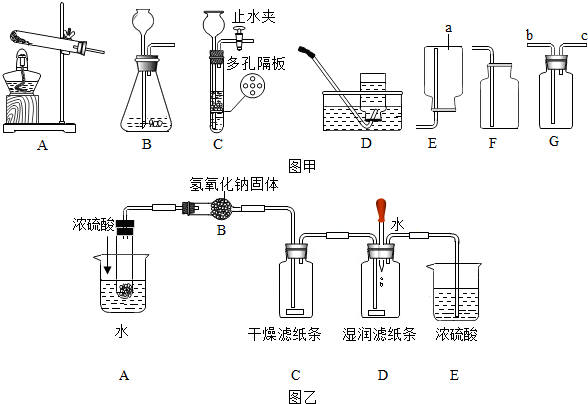
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
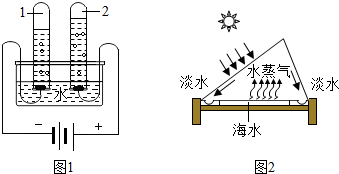
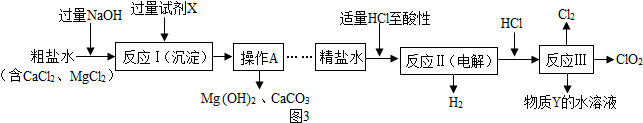
| 氯元素化合价 | ||||
| 化学式 | NaCl | Cl2 | ClO2 | NaClO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验操作 | 实验现象 | 结论 |
| 将黑色粉末过滤、晾干后,分成两份 | ||
| 将其中一份装入硬质玻璃管中,向其中通入CO后,加热,并将生成的气体通入澄清石灰水中 | 澄清石灰水 变浑浊 | 结论I |
| 将另一份置于坩埚中,称其质量为m1,在空气中加热一段时间后冷却,称其质量为m2. | 现象I | 黑色粉末中含Cu |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | H2SO4 NaCl Na2CO3 CaCl2 | B. | HCl NaOH CuSO4Mg SO4 | ||
| C. | Na2CO3 K2SO4 BaCl2 HCl | D. | NaNO3 HCl CaCl2 KOH |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com