
| A. |  闻气体气味 | B. | 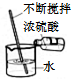 稀释浓硫酸 | C. | 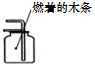 CO2的验满 | D. | 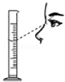 读取液体体积 |
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验方案 | 实验现象 | 结论 |
| ①取一定量的合金粉末用磁铁吸引 | 不能吸引 | 合金中一定不含有铁 |
| ②取步骤①的合金粉末,加入稀盐酸,反应过后,滤渣备用 | 有气泡产生 | 合金中一定含有锌 |
| 取步骤②所得滤渣,加硝酸银溶液 | 溶液有五色变成蓝色 | 合金中一定含有铜 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
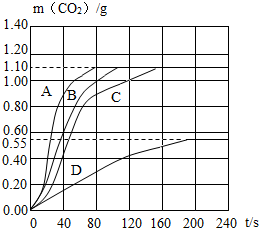
| 实验 编号 | 温度(℃) | 大理石 规格 | 盐酸浓度(均取100mL) | 实验目的 |
| ① | 20 | 粗颗粒 | 20% | (Ⅰ)实验①和②探究盐酸浓度对该反应速率的影响; (Ⅱ)实验①和④探究温度对该反应速率的影响; (Ⅲ)实验①和③探究大理石规格(粗、细)对该反应速率的影响; |
| ② | 20 | 粗颗粒 | 10% | |
| ③ | 细颗粒 | 20% | ||
| ④ | 粗颗粒 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
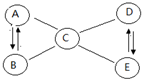 不同类别的物质间能相互反应.如图圆圈内的五种物质为Fe、Fe2O3、H2SO4、NaOH、Na2CO3中的一种.已知A为单质,D可以除去发酵后面团中的酸味.图中“-”表示相连物质可以发生反应,“→”表示一种物质生成另一种物质(部分反应物、生成物及反应条件省略).请完成填空.
不同类别的物质间能相互反应.如图圆圈内的五种物质为Fe、Fe2O3、H2SO4、NaOH、Na2CO3中的一种.已知A为单质,D可以除去发酵后面团中的酸味.图中“-”表示相连物质可以发生反应,“→”表示一种物质生成另一种物质(部分反应物、生成物及反应条件省略).请完成填空.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
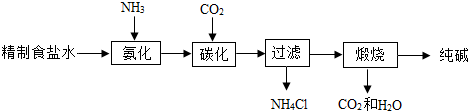
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 维生素和蛋白质 | B. | 无机盐和油脂 | C. | 蛋白质和糖类 | D. | 维生素和糖类 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | NaCl(泥沙):溶解-过滤-蒸发 | |
| B. | CaO固体(CaCO3):高温煅烧 | |
| C. | FeSO4(CuSO4):加入过量铁粉,过滤 | |
| D. | NaCl溶液(Na2SO4):加入过量的氯化钡溶液,过滤 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com