硫酸溶液20克与32.33克氯化钡溶液恰好完全反应,得到50克溶液,则反应后溶液的百分比浓度为 .
【答案】
分析:根据化学方程式计算的步骤有:一设、二写、三找、四列、五答、六查.在本题中,首先根据质量守恒定律求沉淀,再根据沉淀的质量求盐酸的溶质的质量,最后根据质量分数公式求反应后溶液的百分比浓度.
解答:解:根据质量守恒定律,生成沉淀的质量=20g+32.33g-50g=2.33g,
设生成的盐酸的溶质的质量为x,
H
2SO
4+BaCl
2=BaSO
4↓+2HCl
233 73
2.33g x
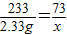
x=0.73g
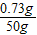
×100%=14.6%
故答案为:14.6%
点评:本考点考查了根据化学方程式的计算,属于质量分数和化学方程式的综合应用,是中考计算题中经常出现的题型.做题时要注意:化学方程式要写正确,始终不要忘记质量守恒定律,还要记牢“遇到差值要想气体”.本考点主要出现在计算题中.

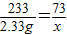 x=0.73g
x=0.73g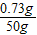 ×100%=14.6%
×100%=14.6%

 全能测控一本好卷系列答案
全能测控一本好卷系列答案