
| A. | 镁 | B. | 铜 | C. | 碳 | D. | 锌 |
分析 根据铁与盐酸反应的化学方程式可以计算出5.6g纯铁能生成0.2g氢气.由于0.2g<0.22g,说明不纯的铁中所含的杂质能与盐酸反应且能产生氢气,而且等质量的铁和所含杂质相比,杂质与盐酸反应产生的氢气多.
解答 解:设5.6g纯铁与盐酸反应生成氢气的质量为x.
Fe+2HCl=FeCl2+H2↑
56 2
5.6g x
$\frac{56}{5.6g}$=$\frac{2}{x}$
解得:x=0.2g<0.22g
说明不纯的铁中所含的杂质能与盐酸反应且能产生氢气,而且等质量的铁和所含杂质相比,杂质与盐酸反应产生的氢气多,由于铜、碳不能与盐酸反应,杂质不可能为铜和碳;由于等质量的镁、锌、铁与盐酸反应时产生的氢气质量由多到少的顺序是:镁>铁>锌,结合上述分析说明杂质为镁.
故选项为:A.
点评 本题考查了混合金属与酸反应生成氢气的质量关系,完成此类题目,可以首先采用极值法,然后采用平均值法进行分析计算.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:解答题
| 物质的质量 | 平均值 |
| 反应前:烧杯+盐酸 | 222.0g |
| 石灰石样品 | 10.0g |
| 反应后:烧杯+滤液 | 226.2g |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 过滤出的不溶物只有铜 | |
| B. | 过滤出的不溶物中一定含有铜,可能含有铁 | |
| C. | 过滤出的不溶物只有铁 | |
| D. | 滤液中一定含有氯化亚铁,可能含有氯化铜 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
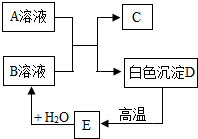 竹海丰富的林竹资源为四川永丰纸业股份有限公司提供了充足的原材料,而造纸工业中常常用到氢氧化钠和碳酸钠等原料.
竹海丰富的林竹资源为四川永丰纸业股份有限公司提供了充足的原材料,而造纸工业中常常用到氢氧化钠和碳酸钠等原料.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
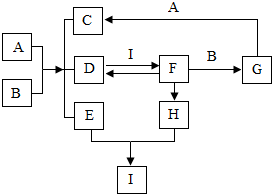 图中表示的是几种常见物质的转化关系(部分反应物、生成物及反应条件省略),已知C为生活中不可缺少的调味品,F为某种建筑材料的主要成分,请回答以下问题:
图中表示的是几种常见物质的转化关系(部分反应物、生成物及反应条件省略),已知C为生活中不可缺少的调味品,F为某种建筑材料的主要成分,请回答以下问题:查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 常见的酸溶液:H2O、HCl、H2SO4 | |
| B. | 常见的黑色固体:CuO、MnO2、Fe3O4 | |
| C. | 常见的有还原性的物质:C、CO、O2 | |
| D. | 常见的碱性溶液:KOH溶液、Na2CO3-溶液、NaOH溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com