
【题目】“比较法”是学习中常用的方法,请在下列横线处填“>”“=”或“<”。
(1)硬度:硬铝(铝的合金)_____铝。
(2)氧元素的化合价:H2O_____H2O2。
(3)等质量的O2和O3中氧原子的个数:O2_____O3。
科目:初中化学 来源: 题型:
【题目】镍在元素周期表中的信息如下图所示,下列有关镍元素的说法不正确的是

A. 原子序数是28 B. 属于金属元素
C. 原子中的质子数是28 D. 相对原子质量为58.69 g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某碳酸钠样品含有少量的硫酸钠,取一定质量的该样品,完全溶解在水中配制成100g溶液,将其全部加入到100g一定质量分数的硫酸溶液中,恰好完全反应,生成的气体全部逸出后,所得溶液质量是195.6g,将溶液蒸干,得到15.6g硫酸钠。
计算:原碳酸钠样品中碳酸钠的质量分数________(计算结果精确到0.1%)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是A、B、C三种物质的溶解度曲线,据图回答:
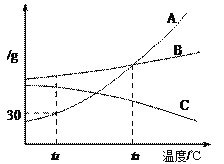
(1)t1℃时A、B、C三种物质的溶解度由大到小的顺序是___________(填写序号,下同)。
(2)t1℃时30gA物质加入到50g水中不断搅拌,形成的溶液质量是_________g。
(3)将t1℃时A、B、C三种物质饱和溶液的温度升高到t2℃时,三种溶液的溶质质量分数由大小关系是______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我们学习过常见气体的实验室制法,知道了制取气体的一般思路和方法
(1)实验室制取气体时,确定发生装置需要考虑的两种因素有_______(填序号)
A.反应物的状态 B.气体的密度
C.反应的条件 D.气体的溶解性
(2)某实验室的仪器柜里有如下仪器:
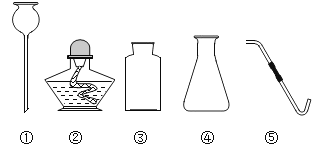
仪器①的名称是________,实验室用大理石和稀盐酸制备并收集二氧化碳时,不可能选择的仪器是______(填序号)
(3)老师提出用碳酸钠粉末与稀盐酸制取二氧化碳,其反应的化学方程式为________.为了完成该实验,有四位同学组装了以下发生装置,你认为最合适的一套装置是_______(填序号),该装置的最大优点是_______.该装置还可以用于实验室制取________.
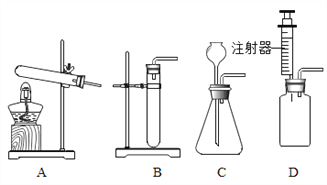
(4)若用50克稀盐酸与10克大理石(含杂质)恰好完全反应生成2.2克二氧化碳,求稀盐酸的质量分数__________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】科学家设想利用太阳能加热器“捕捉CO2”“释放CO2”,实现碳循环,如图所示:
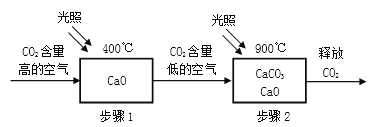
(1)步骤1的化学方程式为______。
(2)为确定步骤2中的碳酸钙是否完全分解,设计的实验步骤为:取少量固体于试管中,滴加过量_______溶液,若观察到试管内______,则分解不完全。
(3)CO2是宝贵的碳氧资源。CO2和H2在一定条件下可直接化合成甲酸(HCOOH),写出该反应方程式___________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在电缆产生过程中会产生一定量的含铜废料。据报道,在通入空气并加热的条件下,铜与稀硫酸反应转化为硫酸铜。
(1)请完成该反应的化学方程式:2Cu+2H2SO4+O2![]() 2CuSO4+2_______
2CuSO4+2_______
(2)若选用的稀硫酸溶质的质量分数为20%,则用50g质量分数为98%的浓硫酸配制该稀硫酸,需加水_____g。
(3)某化工厂现有含铜为80%的废铜屑(假设废铜屑中杂质不参加反应),试计算制取80kg硫酸铜需要废铜屑的质量(写出计算过程及结果)____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是甲、乙两种固体物质在水中的溶解度曲线。下列说法不正确的是
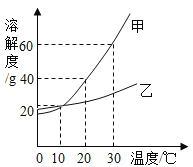
A.10 ℃ 时,甲、乙两种物质的饱和溶液浓度相同
B.保持20 ℃ ,蒸发溶剂可使接近饱和的乙溶液变成饱和溶液
C.30 ℃ 时,将40g 甲物质加人50g水中,充分溶解后溶液的质量为80g
D.10 ℃ 时,将两种饱和溶液升温至30 ℃ ,溶液中溶质的质量分数都增大
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组同学欲除去固体氯化钠中混有的氯化钙,设计实验方案如下,请参与实验并回答问题。
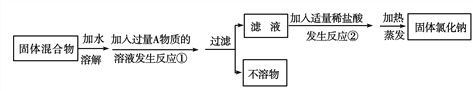
(1)写出A物质的化学式_____________,写出A物质的俗称_____________。
(2)写出反应②的化学方程式_________________________________________。
(3)反应①中加入过量A物质的目的是_________________________________。
反应②中如果加入盐酸也过量,则对所得到的氯化钠纯度________ (填“有”或“没有”)影响。
(4)分离后所得氯化钠的质量与分离前原混合物中氯化钠的质量相比较,结果________ (填“增大”、“不变”或“减小”),其原因是_______________;你认为加入适量盐酸应依据的现象是_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com