
| 106 |
| x |
| 44 |
| 2.2 |
| 117 |
| y |
| 44 |
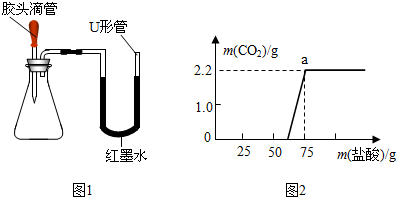
| 2.2g |
| 5.3g |
| 13.3g |
| 40 |
| 8g |
| 58.5 |
| z |
| 5.85g+11.7g |
| 100g+75g-2.2g |


 活力课时同步练习册系列答案
活力课时同步练习册系列答案科目:初中化学 来源: 题型:
| A、Fe、Ag、CuSO4溶液 |
| B、Cu、Ag、FeSO4溶液 |
| C、Fe、Cu、AgNO3溶液、稀盐酸 |
| D、Cu、FeSO4溶液、AgNO3溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
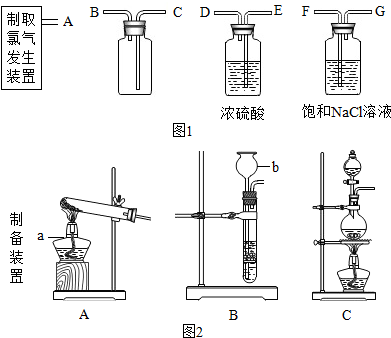 氯气(Cl2)是黄绿色有刺激性气味的气体,有毒.水溶液叫氯水.把品红试纸(染有品红的纸)伸入氯水中,品红褪色.
氯气(Cl2)是黄绿色有刺激性气味的气体,有毒.水溶液叫氯水.把品红试纸(染有品红的纸)伸入氯水中,品红褪色.
| ||
| 实验操作 | 实验现象 | 过程分析 |
| ①把品红试纸伸入水中 | 没有褪色 | 猜想1不成立 |
| ②把品红试纸伸入干燥的氯气中 | 没有褪色 | 猜想2不成立 |
| ③ | 没有褪色 | 猜想3不成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:
 人类社会的生存与发展离不开水,淡水资源和环境问题是困扰人类可持续发展的一个重要因素.当今世界上有80多个国家、约20多亿人口面临淡水危机,其中26个国家的3亿多人口生活在缺水状态中.请回答下列问题:
人类社会的生存与发展离不开水,淡水资源和环境问题是困扰人类可持续发展的一个重要因素.当今世界上有80多个国家、约20多亿人口面临淡水危机,其中26个国家的3亿多人口生活在缺水状态中.请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com