

| 第一次 | 第二次 | |
| 加热纯碱样品的质量 | 30g | 30g |
| 加热后石灰水产生沉淀质量 | 10g | 10g |
| 加入氯化钙溶液的质量 | 50g | 100g |
| 烘干所得沉淀的质量 | M | 20g |
| ||
| 44 |
| 100 |
| p |
| 10g |
| ||
| 168 |
| 44 |
| X |
| 10g |
| 106 |
| 44 |
| Y |
| 4.4g |
| 18 |
| 44 |
| Z |
| 4.4g |
| 111 |
| w |
| 106 |
| n |
| 100 |
| 20g |
| 117 |
| m |
| 30g-16.8g-(21.2g-106g)+23.4g |
| 30g-4.4g-1.8g+100g-20g+96.2g |
| 22.2g |
| 100g |
| 55.5%×p |
| p+q |
| p |
| q |
| 2 |
| 3 |
| ||


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
| 选项 | 物质(括号内为杂质) | 试剂 | 反应类型 |
| A | H2O(H2O2) | 足量MnO2 | 分解反应 |
| B | Ca(OH)2(CaO) | 适量稀盐酸 | 化合反应 |
| C | CO2(CO) | 足量CuO | 置换反应 |
| D | CuO(Cu) | 足量O2 | 复分解反应 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 实验序号 | 实验操作 | 实验现象 | 反应的化学方程式或结论 |
| ① | 将铬投入稀盐酸中 | 铬慢慢溶解,溶液呈蓝色 | Cr+2HCl═CrCl2+H2↑ 铬的金属活动性比金属■强 |
| ② | 将铬投入FeCl2溶液中 | (2) | Cr+FeCl2═CrCl2+Fe |
| ③ | 将铝投入稀■酸中 | 铝迅速溶解,产生气泡 | 2Al+6H■═2Al■+3H2↑ |
查看答案和解析>>
科目:初中化学 来源: 题型:
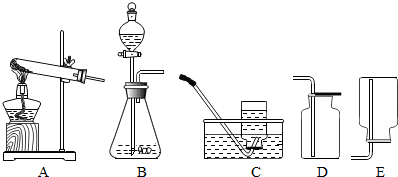
查看答案和解析>>
科目:初中化学 来源: 题型:
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com