
【题目】某化学活动兴趣小组用如图1装置进行木炭还原氧化铜的探究实验,反应一段时间后,,甲中试管内黑色粉末全部变成红色,乙中澄清石灰水变浑浊。
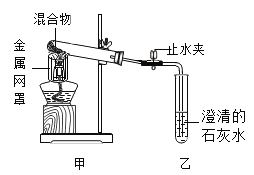
(1)写出木炭还原氧化铜的化学方程式_____________。
(2)待反应结束,先将导气管从石灰水中取出,然后关闭止水夹,让产物自然冷却。若罩不关闭止水夹,可能出现的问题是___________。
[查阅资料]木炭还原氧化铜在反应过程中,有可能生成氧化亚铜(Cu2O),氧化亚铜为红色固体。
[探究一]同学们对反应后玻璃管中的红色粉末是否含有氧化亚铜展开探究,已知氧化亚铜能与稀硫酸反应:![]() 。取少量红色固体于试管中,加入过量的稀硫酸,观察到______________,说明红色粉末中含有Cu2O。
。取少量红色固体于试管中,加入过量的稀硫酸,观察到______________,说明红色粉末中含有Cu2O。
[探究二]有同学提出,木炭还原氧化铜的过程中,除了会生成氧化亚铜,还有可能生成一氧化碳,他的依据是___________。于是他重复实验并收集反应生成的气体,将气体干燥后,再通过灼热的氧化铜,观察到有___________,色固体生成,说明有CO生成。
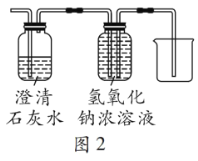
[反思与评价]根据以上探究,有同学认为原实验装置存在不足,于是将乙装置改进为如图2所示,改进后装置的优点是__________。
【答案】 铜重新被氧化成氧化铜(或红色的铜重新被氧化成黑色的氧化铜等合理即可) 溶液变蓝 化学反应前后,元素的种类不变(或质量守恒定律) 红 吸收二氧化碳并收集一氧化碳,防止污染空气
铜重新被氧化成氧化铜(或红色的铜重新被氧化成黑色的氧化铜等合理即可) 溶液变蓝 化学反应前后,元素的种类不变(或质量守恒定律) 红 吸收二氧化碳并收集一氧化碳,防止污染空气
【解析】
(1)木炭还原氧化铜时,生成铜和二氧化碳,反应的化学方程式为 ;
;
(2)实验结束后,先将导气管从石灰水中取出,然后关闭止水夹,让产物自然冷却,若不关闭止水夹,空气进入试管中,铜重新被氧化成氧化铜(或红色的铜重新被氧化成黑色的氧化铜等)
[探究一]
根据进行的操作、得出的结论,结合[查阅资料]氧化亚铜能和稀硫酸反应生成硫酸铜溶液,故观察到的现象是溶液由无色变为蓝色。
[探究二]
木炭还原氧化铜的过程中,除了会生成氧化亚铜,还有可能生成一氧化碳,原因是化学反应前后,元素的种类不变。一氧化碳可与灼热的氧化铜反应生成铜和二氧化碳,则观察到的现象是有红色固体生成。
[反思与评价]
根据探究可知木炭还原氧化铜时有CO生成,CO会污染空气,改进后装置中的氢氧化钠浓溶液既可吸收CO2,又可将溶液排出达到收集CO的目的,防止污染空气。


科目:初中化学 来源: 题型:
【题目】如图为实验室常见的气体制备、收集和性质的实验装置,据图回答。
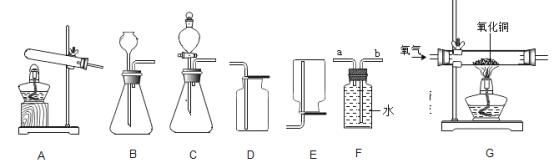
(1)推出C、D装置中标号仪器名称:X_____、Y_____。
(2)O2的制取方法有多种,若用加热氯酸钾的方法制取O2,应选用的发生装置为_____(填装置序号,下同),反应方程式为:_____。
(3)小海同学在装置B中加入15%的过氧化氢溶液和二氧化锰制取氧气。
①若用F装置收集氧气,氧气应从_____(填“a”或“b”)端通入。
②实验中发现不能得到平稳的氧气流。小涛同学提出可以从两个方面加以改进:
一是将制取的装置B换为上图中的装置_____;
二是将过氧化氢溶液加水稀释。如果在80g溶质质量分数为15%的过氧化氢溶液中加入70克水,则所得溶液的溶质质量分数为_____。
(4)实验室用加热氯化铵和氢氧化钙固体混合物制取氨气,生成氨气的化学方程式为_____,为探究氨气的性质,小红用图中G装置进行氨气与氧化铜反应的实验,实验中观察到黑色氧化铜粉末变成红色。
(提出问题)得到的红色粉末是什么?
查阅资科:Cu2O是红色,易与稀硫酸反应:![]()
(猜想假设)红色粉末是①Cu②Cu2O③_____
(设计实验)小明设计如下实验验证红色粉末中是否含有Cu2O
实验步骤 | 实验现象 | 实检站论 |
取红色粉末于试管中,加入足量稀硫酸 | _____ | 红色粉末中含有Cu2O |
(实验反思)小明设计的实验无法证明红色粉末中是否含有Cu,原因是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知M、N两种固体物质的溶解度曲线如图所示,下列说法正确的是(____)

A t1°C时等质量的M、N两种物质的溶液中溶质质量相等。
B t2°C时15gM加入到50g水中,充分溶解得到65g溶液
C 若M物质中含有少量N物质,可采用降温结晶的方法提纯M物质
D 将t2°C时N的饱和溶液降温至t1°C时,溶液中溶质的质量_____(填“增大” “减小” 或“不变")
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】经父母许可后,小明从家里拿了一些治疗胃病的药片到实验室进行成分探究。说明书告知该胃药可以治疗胃酸过多,其主要成分是氢氧化铝和碳酸镁中的一种或两种。
(提出问题)该胃药的具体成分如何?
(查阅资料)
a.碳酸镁与碳酸钙性质类似
b.氢氧化铝受热分解生成氧化铝和水
c.无水硫酸铜遇水变蓝:![]()
(实验探究)
(1)小明同学取少量该胃药于试管中,加入适量的稀盐酸,观察有气泡产生。该胃药中一定含有的物质名称是___________,反应化学方程式为_____________。
(2)为进一步确定该胃药的主要成分,小明的甲、乙两位同学利用下图所示装置(气密性良好)分别设计了两套不同的实验方案。
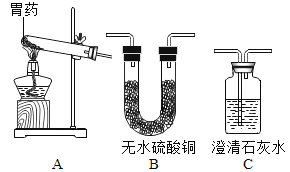
方案①甲同学按照A→B→C顺序连接装置,点燃酒精灯加热试管。观察B中无明显现象,C中澄清石灰水变浑浊。
方案②乙同学按照A→C→B顺序连接装置,点燃酒精灯加热试管。观察C中澄清石灰水变浑浊,B中物质由白色变成蓝色。你认为上述①②两个实验方案合理的是________________。
(3)在上述方案①②实验过程中所有发生反应的化学方程式为___________、________。
(得出结论)
(4)根据上述实验探究,确定胃药的要成分化学式为_____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2019年1月嫦娥四号成功着陆在月球背面南极------------艾特肯盆地冯卡门撞击坑的预选着陆区。撞击坑内的钍、氧化铁、二氧化钛等含量较高,是一个巨大的矿产资源库。
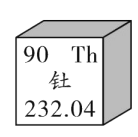
(1)已知钍经过中子轰击,可得铀-233,是潜在的核燃料。它在元素周期表中的信息如图所示,由此可知,钍原子核中质子数为______,钍元素的相对原子质量为__________。
(2)二氧化钛被认为是现今世界上性能最好的一种白色颜料,也是冶炼钛、钛合金的重要原料。钛合金具有比钛更优良的特性,表现在___________ (写一条) ,冶炼钛过程中发生的一个反应为TiO2+2Cl2+2C=TiCl4+2X,由此可推断出X的化学式为_____________。
(3)赤铁矿的主要成分是氧化铁,它是炼铁的主要原料。已知铁原子的核外电子排布如图所示,由此可知,Y=___________。 对比1 ~20号元素的原子核外电子排布规律,可发现铁原子的核外电子排布的不同点是__________。

查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】阅读下面短文,回答问题。
页岩气
随着社会对清洁能源需求不断扩大,天然气价格不断上涨,人们对页岩气的认识迅速提高。特别是水平井与压裂技术水平不断进步,人类对页岩气的勘探开发正在形成热潮。页岩气是指赋存于富有机质泥页岩及其夹层中,以吸附和游离状态为主要存在方式的非常规天然气,成分以甲烷为主,是一种清洁、高效的能源资源和化工原料,主要用于居民燃气、城市供热、发电、汽车燃料和化工生产等,用途广泛。我国页岩气资源潜力大,初步估计我国页岩气可采资源量在36.1万亿立方米,与常规天然气相当。
(1)页岩气属于________(填“可再生”或“不可再生”)能源。
(2)页岩气燃烧是将化学能转化为___________。
(3)若页岩气的热值为![]() ,则燃烧5L页岩气放出的热量为___________J。
,则燃烧5L页岩气放出的热量为___________J。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】薄荷醇(化学式为C10H20O)可用于糖果、饮料的加香.下列有关薄荷醇的说法正确的是
A. 薄荷醇的相对分子质量为156g
B. 薄荷醇由10个碳原子、20个氢原子和1个氧原子构成
C. 薄荷醇中碳元素、氢元素和氧元素的质量比为10:20:1
D. 薄荷醇中碳元素的质量分数约为76.9%
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据如图判断以下说法中正确的是( )

A.钙元素为非金属元素
B.“Ca”既可表示金属钙,又可表示一个钙元素
C.钙离子的核外电子数为18
D.钙的相对原子质量是40.08g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学为探究生石灰暴露空气中的变质情况,设计如下实验:称取生石灰w,露置空气一段时间后,所得粉末A的质量为1.2w,加入足量稀盐酸,生成气体B,依次通入浓硫酸,足量澄清石灰水,得到沉淀0.25w。推断粉末A的组成________(写清楚成分及其对应质量),计算粉末A 中氧化钙的质量分数________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com