
| 序号 | 实验目的 | 实验过程 |
| A | 证明变质 | 取少量溶液,滴加盐酸,将生成的气体通入石灰水 |
| B | 确定成分 | 取少量溶液,加入石灰水,过滤,向滤液中滴加酚酞溶液 |
| C | 测定纯度 | 取一定量溶液,加入盐酸,用氢氧化钠固体吸收气体,称量 |
| D | 除去杂质 | 取溶液,滴加氯化钙溶液至恰好完全反应,过滤 |
| A. | A | B. | B | C. | C | D. | D |
分析 A、氢氧化钠吸收空气中二氧化碳生成碳酸钠而变质,证明变质即证明氢氧化钠溶液中含有碳酸钠;碳酸盐的检验方法是滴加盐酸,将产生气体通入澄清石灰水;
B、已变质的氢氧化钠溶液中含有碳酸钠,确定成分即检验碳酸钠和氢氧化钠的存在;
C、变质的氢氧化钠溶液为碳酸钠的氢氧化钠的混合溶液,测定纯度即测定氢氧化钠或碳酸钠的含量;
D、氢氧化钠溶液吸收空气中二氧化碳生成的碳酸钠即杂质,除去杂质即去除混合溶液中的碳酸钠.
解答 解:
A、证明变质即证明氢氧化钠溶液中含有碳酸钠,根据碳酸钠可与盐酸反应放出二氧化碳,采取滴加盐酸并将生成的气体通入澄清石灰水的方法,观察到石灰水变浑浊时,即可证明溶液中混有碳酸钠;故A正确;
B、确定成分即检验碳酸钠和氢氧化钠的存在,采取加入石灰水与碳酸钠反应生成碳酸钙沉淀和氢氧化钠,过滤后的溶液中含有反应生成的氢氧化钠,此时滴加酚酞变红不能证明原溶液中含有氢氧化钠;故B不正确;
C、测定纯度即测定氢氧化钠或碳酸钠的含量,采取加入盐酸与碳酸钠反应放出二氧化碳,使用固体氢氧化钠吸收放出的二氧化碳,通过称重测定放出二氧化碳的质量;但由于氢氧化钠还能吸收水,因此所测得重量并非二氧化碳的质量;故C错误;
D、除去杂质即去除混合溶液中的碳酸钠,滴加氯化钙溶液时,氯化钙与碳酸钠反应生成碳酸钙和氯化钠,氯化钠是溶于水的,所以在除去碳酸钠后,有生成了新的杂质氯化钠,故D错误;
故选A.
点评 利用氢氧化钠与碳酸钠性质不同及变化规律的不同,选取恰当的试剂,可以检验、测定、除去氢氧化钠溶液中的碳酸钠.


科目:初中化学 来源: 题型:解答题
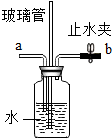 点燃不纯的可燃性气体可能发生爆炸.如图是某同学的改进装置:
点燃不纯的可燃性气体可能发生爆炸.如图是某同学的改进装置:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 化学与健康 ①食用鲜黄瓜-可大量补钙 ②人体缺铁-易患贫血病 | |
| B. | 化学与生活 ①减轻车内异味-开窗通风 ②防止食品受潮-用氧化钙做干燥剂 | |
| C. | 化学与安全 ①重金属盐中毒-喝鲜牛奶解毒 ②煤气泄漏-关闭阀门,严禁烟火 | |
| D. | 化学与环境 ①使用乙醇汽油-减少空气污染 ②合理使用农药、化肥-减少水污染 |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
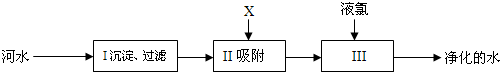
| A. | 步骤Ⅰ可除去难溶性杂质 | B. | X试剂可以是明矾 | ||
| C. | 步骤Ⅲ可杀菌、消毒 | D. | 净化后的水是纯净物 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 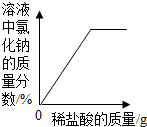 向一定的NaOH溶液中滴加稀HCl | |
| B. | 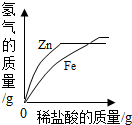 向相同质量的铁粉和锌粉中分别加入足量稀盐酸 | |
| C. | 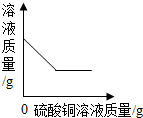 向一定量的铁粉中不断加入硫酸铜溶液 | |
| D. | 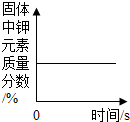 加热一定质量的高锰酸钾 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
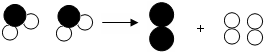
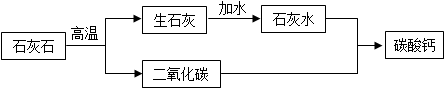
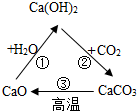 完成下列反应的化学方程式,并回答有关问题,请你用化学方程式表示如图中的三个化学反应
完成下列反应的化学方程式,并回答有关问题,请你用化学方程式表示如图中的三个化学反应查看答案和解析>>
科目:初中化学 来源: 题型:解答题

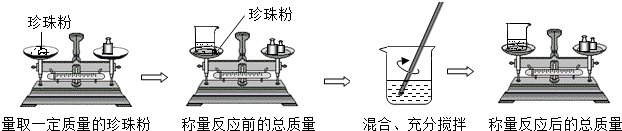
| 组别 | 珍珠粉的质量/g | 反应前的总质量/g | 反应后的总质量/g |
| 甲 | 1.25 | 151.25 | 150.81 |
| 乙 | 12.5 | 162.5 | 158.1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com