
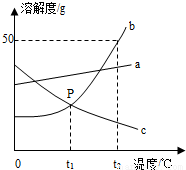
 ×100%,所以与溶解度有关,因为t2℃,a、b、c三种物质的溶解度大小是:b>a>c,所以它们饱和溶液的质量分数也是:b>a>c;
×100%,所以与溶解度有关,因为t2℃,a、b、c三种物质的溶解度大小是:b>a>c,所以它们饱和溶液的质量分数也是:b>a>c;

 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案科目:初中化学 来源: 题型:
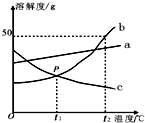 根据如图中a、b、c三种物质的溶解度曲线,回答下列问题:
根据如图中a、b、c三种物质的溶解度曲线,回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:
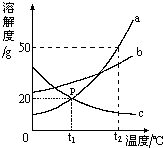 请根据如图中a、b、c三种物质的溶解度曲线,回答下列问题:
请根据如图中a、b、c三种物质的溶解度曲线,回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:
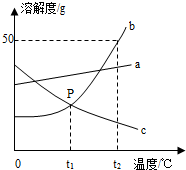 (2012?兰州)根据如图中a、b、c三种物质的溶解度曲线,回答下列问题:
(2012?兰州)根据如图中a、b、c三种物质的溶解度曲线,回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:
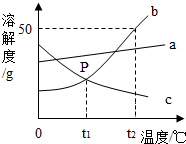 (2013?黄石模拟)(1)用化学符号表示:
(2013?黄石模拟)(1)用化学符号表示:| +2 |
| Mg |
| +2 |
| Mg |
查看答案和解析>>
科目:初中化学 来源: 题型:
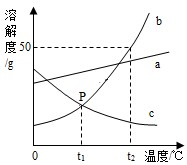 根据如图中a、b、c三种物质的溶解度曲线,回答下列问题:
根据如图中a、b、c三种物质的溶解度曲线,回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com