
| A. | A | B. | B | C. | C | D. | D |
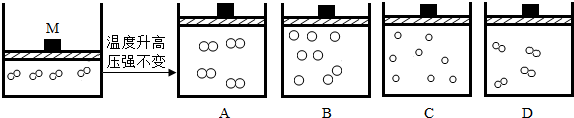
分析 氮气不活泼,在3000℃时仅有0.1%的分子分裂.在0℃常压下,向密闭容器M中充入一定量的氮气,而后升高温度但不超过3000℃,且压强不变,该密闭容器的体积增大了一倍,经分析可知,此时主要发生物理变化,氮气分子极少数分解,即分子大小不变,分子数目基本不变化,主要原因是分子之间的间隙变大了一倍,气体体积增大一倍.
解答 解:A、分子体积增加了,而上述变化中分子大小不变,只是间隙变大,故与题意不符,所以错误.
B、分子多数破裂成了原子,且分子体积增加了,而该变化主要是物理变化,在物理变化过程中分子本身不变,与题意不符,所以错误.
C、分子全部破裂了,该变化主要是物理变化,在物理变化过程中分子本身不变,与题意不符,所以错误.
D、主要是分子之间的间隙变大了一倍,而分子大小没变,分子数目也基本不变,与题意相符,所以正确.
故选D.
点评 本题考查的是物理变化时分子的间隔变化特点,根据已有的分子间隔的知识是正确解答本题的关键.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
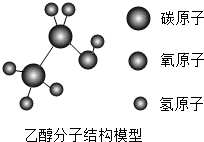 小麦、玉米等经过发酵、蒸馏制得的乙醇被称为“绿色汽油”.乙醇的分子结构如图所示,则下列叙述正确的是( )
小麦、玉米等经过发酵、蒸馏制得的乙醇被称为“绿色汽油”.乙醇的分子结构如图所示,则下列叙述正确的是( )| A. | 乙醇分子是由3种元素组成的有机物 | |
| B. | 乙醇中碳、氧元素的质量比为3:2 | |
| C. | 一个乙醇分子是由10个原子构成的 | |
| D. | 乙醇中氧元素的质量分数最大 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com