
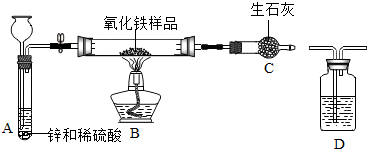
| 实验现象 | 化学方程式 |
| A中反应产生大量气泡; | A中:Zn+H2SO4═ZnSO4+H2↑. |
| B中红色粉末逐渐变黑色; | B中:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2. |
| 反应前 | 氧化铁完全反应后 | |
| ①组 | B:玻璃管质量32.4g,氧化铁样品的质量10.0g | B:玻璃管和管内固体物质的质量40.0g |
| ②组 | C:干燥管和生石灰质量40.Og | C:干燥管和管内固体物质的质量43.0g |
分析 (1)氢气易燃易爆,实验开始先通氢气;实验结束后,为防止铁被氧化,停止加热后还要通入氢气.
(2)由图可知,氢气与氧化铁反应推断现象,则根据反应原理写出化学方程式;
(3)根据反应可知:氧化铜被氢气还原生成铜和水,故质量应该减少,可以据此作答;
(4)根据分析第二组实验结果大于氧化铜的原因可能是反应带出了部分水,使质量增加,故只要加入一个干燥装置即可.
解答 解:(1)实验开始时,先通入氢气,待试管中的空气被排净后,再给氧化铁加热,以防试管内的混合气体受热发生爆炸;实验结束时,先熄灭酒精灯,待试管冷却后,再停止通氢气,目的是使还原出来的铁在氢气环境下冷却,防止空气进入试管中致使灼热的铁被再度氧化,导致实验失败.
(2)氢气与氧化铁反应生成铁粉,B中红色粉末逐渐变黑色;方程式为:Fe2O3+3H2$\frac{\underline{\;\;△\;\;}}{\;}$2Fe+3H2O.
(3)第二组实验结果大于氧化铜的原因可能是反应带出了部分水,使质量增加,使得计算结果不准确;所以选①组
根据氧化铜和氢气的反应可以知道:氧化铁中的氧元素和氢气中氢元素结合生成了水,所以固体的质量应该减少;
设:样品中氧化铁的质量为x.
Fe2O3+3H2$\frac{\underline{\;\;△\;\;}}{\;}$2Fe+3H2O 固体减少
160 112 160-112=48
x 32.4g+10g-40g=2.4g
则$\frac{160}{x}=\frac{48}{2.4g}$,解得x=8.0g
样品中氧化铁的质量分数为:$\frac{8.0g}{10.0g}$×100%=80%;
(4)根据分析第二组实验结果大于氧化铜的原因可能是反应带出了部分水,使质量增加,所以应该在A和B之间加一个干燥装置;装置中加入浓硫酸.
故答案为:(1)排尽空气,防止加热时发生爆炸;
(2)红色;Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2
(3)①;80%
(4)AB;浓硫酸.
点评 此题是一道综合题,解题的重点质量守恒定律等知识进行的计算,是一道能训练学生思维的综合题.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
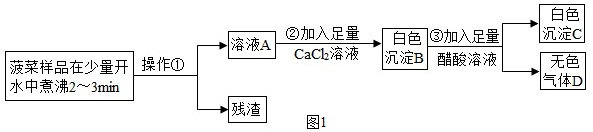
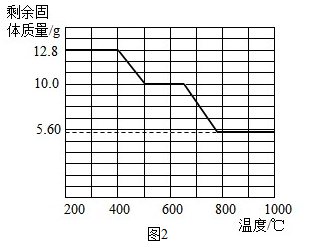
| 实验操作 | 实验现象 | 实验结论 |
| 取少量固体于试管中,加入适量的水,用手触摸试管壁;静置后取上层清液,滴加无色酚酞试液. 取不溶物于试管中,加入足量的稀盐酸,将气体通入澄清石灰水 | 试管壁发烫,溶液变红 有气泡冒出,澄清石灰水变浑浊. | 该固体中含有CaO. 该固体中含有CaCO3. 剩余固体的成分为CaO和CaCO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验步骤 | 实验现象 | 实验结论 |
| 取氢氧化钙样品少量,研细后加适量蒸馏水充分混合后静置,取少量上层清液,滴加1~2滴无色酚酞试液 | 该样品还含有氢氧化钙 |
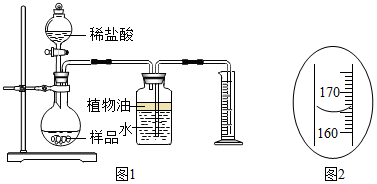
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 猜测1 | 猜测2 | 猜测3 |
| 只有CO | 只有 CO2 | 含有CO和CO2 |
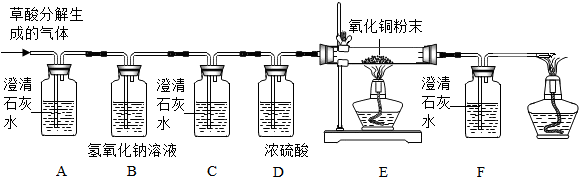
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com