
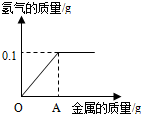
 将足量的铁放于50g稀硫酸中,充分反应后,得到的实验数据绘制成图象如图.
将足量的铁放于50g稀硫酸中,充分反应后,得到的实验数据绘制成图象如图.| 溶质的质量 |
| 溶液质量 |
| 56 |
| y |
| 98 |
| x |
| 2 |
| 0.1g |
| 4.9g |
| 50g |


 金钥匙试卷系列答案
金钥匙试卷系列答案科目:初中化学 来源: 题型:
| 第一次 | 第二次 | 第三次 | |
| 加入稀硫酸的(g) | 24.50 | 24.50 | 24.50 |
| 烧杯中剩余固体(g) | 5.80 | 3.00 | 0.20 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
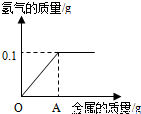
 将足量的铁放于50g稀硫酸中,充分反应后,得到的实验数据绘制成图象如图.
将足量的铁放于50g稀硫酸中,充分反应后,得到的实验数据绘制成图象如图.查看答案和解析>>
科目:初中化学 来源:2010-2011学年山东省日照市莒县九年级(上)期末化学试卷(解析版) 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com