
分析 锌与稀硫酸反应生成硫酸锌和氢气,由生成氢气的质量,由反应的化学方程式列式计算出生成硫酸锌的质量、参加反应的硫酸的质量、参加反应的锌的质量,进而计算出反应前稀硫酸中溶质的质量分数.
解答 解:设生成硫酸锌的质量为x,参加反应的硫酸的质量为y,参加反应的锌的质量为z,
Zn+H2SO4═ZnSO4+H2↑
65 98 161 2
z y x 0.4g
$\frac{161}{2}=\frac{x}{0.4g}$ x=32.2g
$\frac{98}{2}=\frac{y}{0.4g}$ y=19.6g
$\frac{65}{2}=\frac{z}{0.4g}$ z=13g
生成硫酸锌溶液的质量为32.2g÷20%=161g.
反应前稀硫酸中溶质的质量分数为$\frac{19.6g}{161g+0.4g-13g}$×100%≈13.2%.
答:反应前稀硫酸中溶质的质量分数为13.2%.
点评 本题难度不大,掌握利用化学方程式与溶质质量分数的综合计算即可正确解答本题,解题时要注意解题的规范性.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
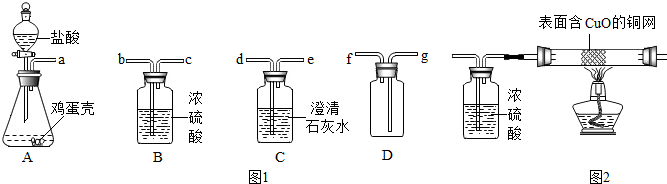
科目:初中化学 来源: 题型:实验探究题
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
| 溶解度/g | KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | |
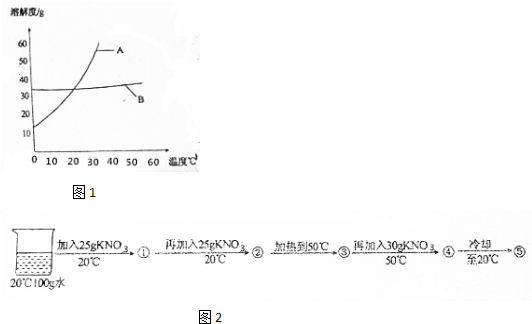
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 如图为某医用葡萄糖注射液标签的一部分.
如图为某医用葡萄糖注射液标签的一部分.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
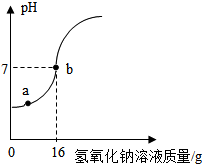 欲测定一瓶标签破损的稀硫酸的溶质质量分数.现取10g稀硫酸样品,将溶质质量分数为5%的氢氧化钠溶液逐滴加入到样品中,进行了数字化实验,边加边搅拌,随着氢氧化钠溶液加入,计算机描绘出了整个实验过程中溶液pH的变化图象(如图所示).
欲测定一瓶标签破损的稀硫酸的溶质质量分数.现取10g稀硫酸样品,将溶质质量分数为5%的氢氧化钠溶液逐滴加入到样品中,进行了数字化实验,边加边搅拌,随着氢氧化钠溶液加入,计算机描绘出了整个实验过程中溶液pH的变化图象(如图所示).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com